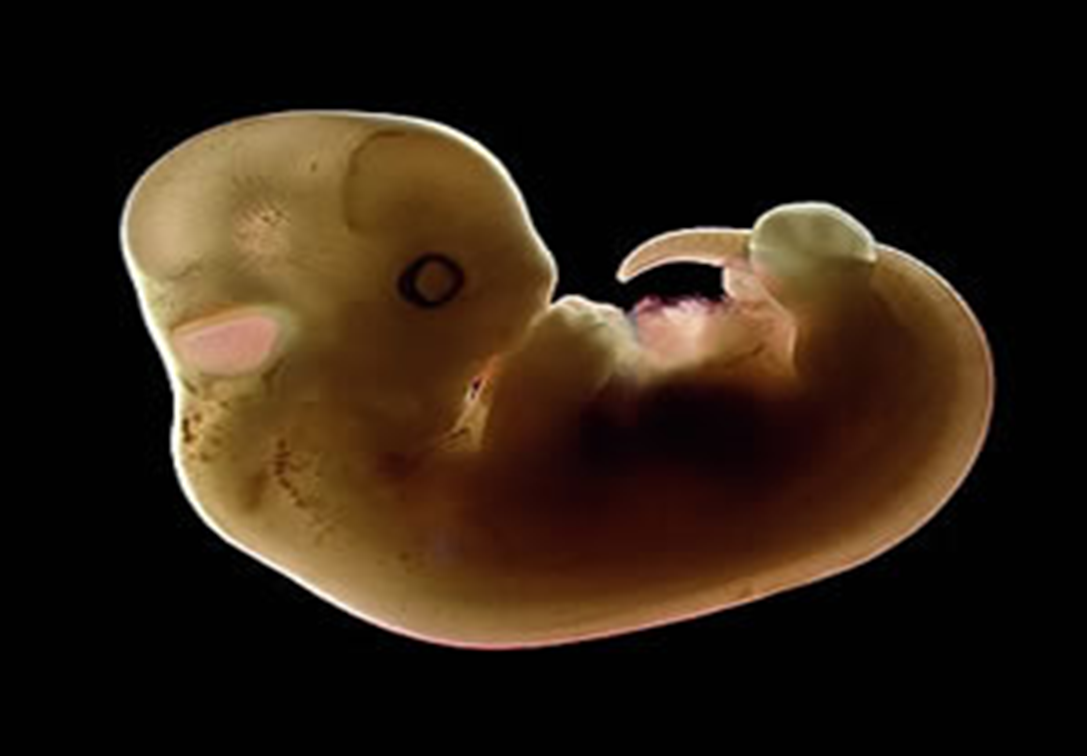
Embrião entre a 5ª e a 8ª semana
https://www.ncbi.nlm.nih.gov/books/NBK557601/
Aatsha PA (1); Tafline C. Arbor (2); Kewal Krishan (3)
Afiliações
1 Faculdade de Medicina do Governo de Thrissur, Keralla, Índia
2 Escola de Medicina da Universidade Wake Forest, Carolina do Norte, EUA
3 Departamento de Antropologia (Centro de Estudos Avançados da UGC), Universidade de Panjab, Chandigarh, Índia
28 ago 2023
[Nota do Website: Resolvemos publicar esse trabalho científico sobre a embriogênese para que os leitores possam captar a profundidade das ações dos disruptores endócrinos sobre os seres humanos que ainda nem nasceram. Temos que recuperar o conhecimento de que essas moléculas sintéticas alteram a formação saudável dos fetos, sejam XX-fêmeas, sejam os XY-machos. Como elas agem como se fossem hormônios -FALSOS-, acabam gerando disfunções definitivas e permanentes a esses seres que ainda estão em formação. E, dramaticamente estão numa situação onde são totalmente indefesos e completamente vulneráveis. E como elas atuam em níveis hormonais, ou seja, em doses infinitesimais, a agressão ficará destrutível. Por isso não seguem os conceitos corriqueiros da toxicologia convencional, da Idade Média de Paracelsus, onde a dose define seus efeitos. É impossível ter quaisquer alterações após o nascimento e mesmo durante a sua formação fetal, caso ocorram essas disfunções. E essa é a nossa responsabilidade, pessoal e coletiva, em relação ao futuro de todos os seres, humanos ou não-humanos!].
Introdução
O desenvolvimento de um sistema reprodutivo funcional é uma das características mais críticas de um organismo, pois está diretamente relacionado à sua aptidão genética. O legado genético de um indivíduo é transmitido às gerações subsequentes por meio das células germinativas presentes nas gônadas em desenvolvimento. [1] O desenvolvimento sexual envolve dois processos distintos: a determinação do sexo e a diferenciação sexual. A determinação do sexo é a atribuição do sexo que direciona o zigoto indiferenciado a se desenvolver em um indivíduo sexualmente dimórfico (em direção ao sexo masculino ou feminino). [2] Em humanos, o sexo cromossômico é determinado na fertilização, quando um espermatozoide contribui com um cromossomo X ou Y para o cromossomo X no oócito.
A diferenciação sexual é o processo e o caminho de desenvolvimento que leva ao desenvolvimento de fenótipos masculinos ou femininos a partir de estruturas embrionárias indiferenciadas. A diferenciação sexual geralmente se desenvolve ao longo de um caminho consistente com o sexo cromossômico do embrião. A diferenciação sexual envolve múltiplos níveis: cromossômico, gonadal, hormonal, fenotípico e psicológico. No nível genético, o sexo cromossômico é determinado pelo complemento cromossômico após a fertilização, onde XY indica um sexo cromossômico masculino e XX indica um sexo cromossômico feminino. Até aproximadamente a sexta semana pós-fertilização, nenhuma diferença sexual é observável em um concepto cromossomicamente masculino ou feminino. As gônadas bipotenciais são as primeiras a se diferenciarem e são morfologicamente indistinguíveis no início do desenvolvimento. A diferenciação gonadal em ovários ou testículos é uma parte importante do desenvolvimento sexual, pois uma gônada funcional e os hormônios que ela produz impactam o desenvolvimento e a diferenciação dos genitais internos, genitais externos e características sexuais secundárias de um indivíduo. [3] [4]
Desenvolvimento
Nos seres humanos, o sexo biológico é determinado pelo conjunto de cromossomos sexuais que fornecem instruções para que um embrião indiferenciado se forme seguindo a linhagem masculina ou feminina. Inicialmente, um concepto é sexualmente distinto apenas pelo seu cariótipo, em que os machos possuem cromossomos sexuais XY e as fêmeas, XX. A diferenciação sexual é o processo subsequente, dinâmico e complexo, regulado por diversas causas genéticas e ambientais, que diferencia as gônadas indiferenciadas, os genitais internos e os genitais externos, seguindo a linhagem masculina ou feminina.
Diferenciação Gonadal
A diferenciação gonadal é o processo que se inicia com uma gônada bipotencial indiferenciada e termina com seu desenvolvimento em testículo ou ovário. Genes específicos induzem a diferenciação gonadal, que começa por volta da quinta semana de desenvolvimento pós-fertilização com a formação do primórdio gonadal. [3] [5] [6] Um mesotélio espessado se desenvolve medialmente ao mesonefro e prolifera para formar a crista urogenital em cada lado do embrião. As cristas urogenitais pareadas aparecem como cristas longitudinais na quarta semana pós-fertilização e são compostas de mesoderma intermediário coberto por epitélio celômico.
As cristas urogenitais são precursoras comuns que contribuem para a formação do sistema urinário, do sistema genital e do córtex adrenal. A crista urogenital divide-se em um componente urinário e um componente adrenogonadal. Para este último, células especializadas formam-se em estreita proximidade, constituindo a crista gonadal e, em última instância, contribuindo para a formação das células esteroidogênicas das gônadas adrenais e das glândulas adrenais. Além disso, cordões epiteliais digitiformes, os cordões sexuais primitivos ou gonadais, desenvolvem-se no primórdio gonadal e crescem em direção ao mesênquima. Nesse estágio do desenvolvimento, as gônadas indiferenciadas, porém bipotenciais, são compostas por um córtex externo e uma medula interna, com destinos distintos na diferenciação gonadal masculina e feminina. Tanto em embriões XX quanto XY, as células germinativas primordiais migram da vesícula umbilical ao longo do mesentério dorsal para alcançar a região das cristas gonadais e são incorporadas aos cordões gonadais. As células germinativas primordiais darão origem, posteriormente, a oócitos e espermatozoides durante o desenvolvimento.
TODAS AS IMAGENS FORAM ACRESCENTADAS PELA TRADUÇÃO
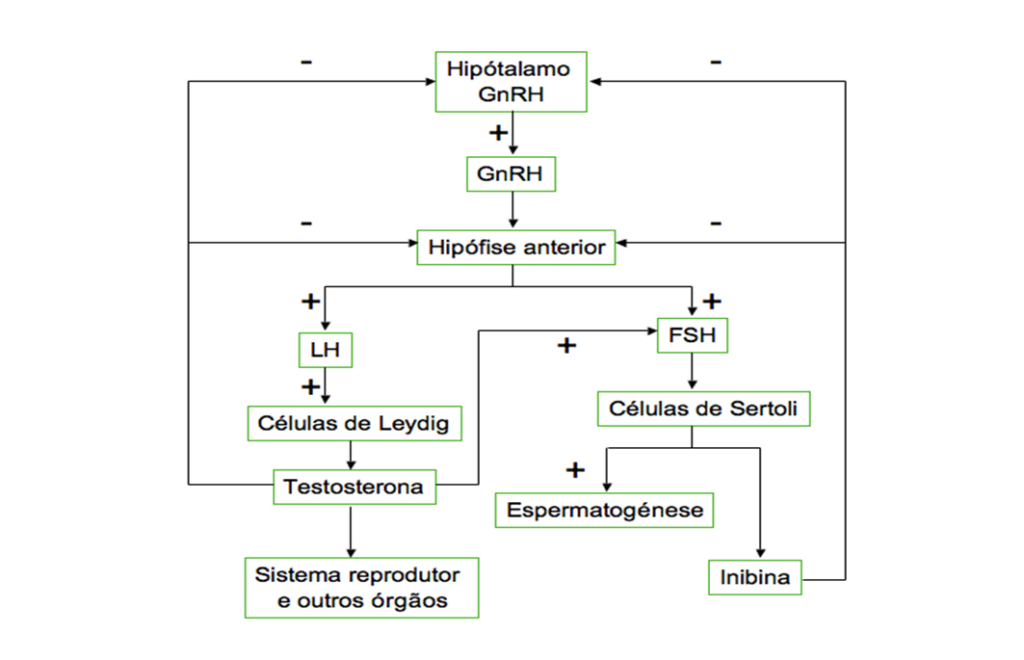
Hipotálamo é quem controla a homeostase (equilíbrio=saúde) do corpo. A hipófise ou pituitária é considerada a ‘glândula mestra’ na determinação endócrina (hormonal) do corpo. (Todas as imagens acima foram agregadas pela tradução).
Testículo
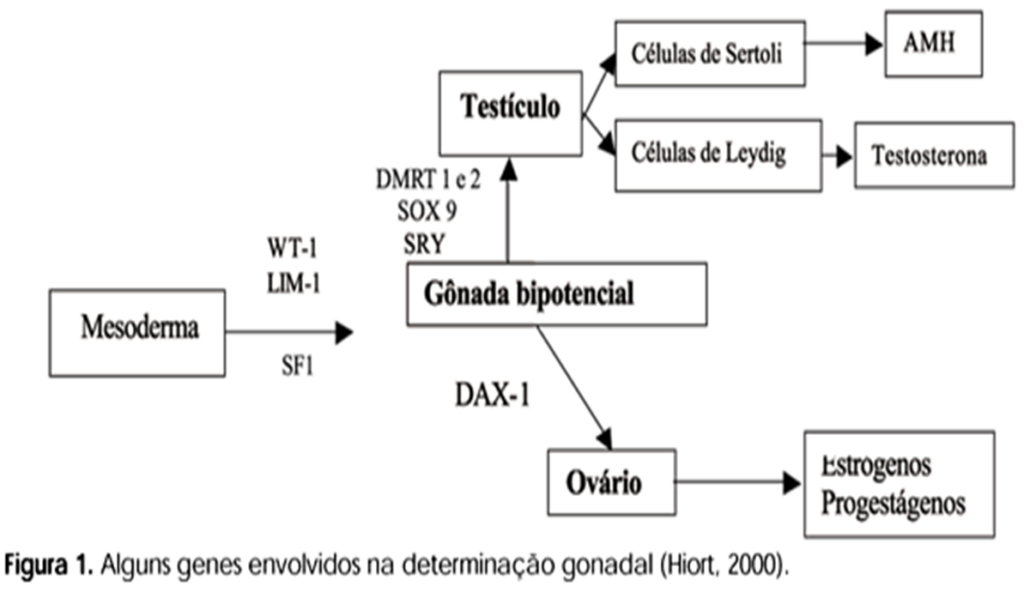
Se um embrião for cromossomicamente masculino (46 XY), a gônada bipotencial se diferencia em testículos sob a influência do gene SRY. O gene SRY é um gene de éxon único e codifica um fator de transcrição chamado proteína da região determinante do sexo Y (proteína SRY), também conhecido como fator determinante dos testículos (TDF). A proteína SRY, ou TDF, é um gene de determinação sexual que direciona a diferenciação gonadal masculina. A expressão do gene SRY auxilia na diferenciação das células de Sertoli, o que posteriormente resulta na produção da substância inibidora mülleriana (MIS) ou hormônio antimülleriano (AMH). O SOX9 também auxilia na diferenciação das células de Sertoli, sendo regulado positivamente pelo gene SRY. É uma etapa crítica no início do desenvolvimento testicular. [7]
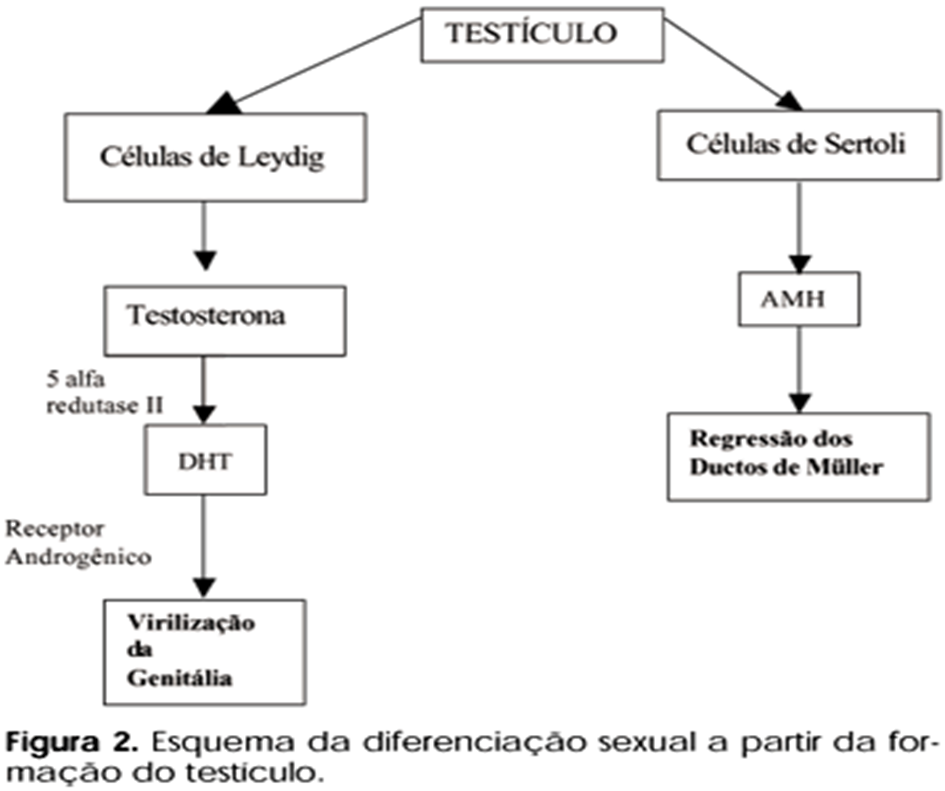
No início do desenvolvimento gonadal masculino, o TDF induz a condensação dos cordões gonadais e a formação de canais anastomóticos, resultando na formação da rete testis na medula da gônada indiferenciada. A túnica albugínea se forma e separa os cordões gonadais, ou cordões sexuais primitivos, do epitélio superficial, sendo um indicador observável do desenvolvimento dos testículos. Os cordões gonadais passam a ser denominados cordões seminíferos após o desenvolvimento da túnica albugínea e, eventualmente, formam os túbulos seminíferos, os túbulos retos e a rete testis. Os túbulos seminíferos são separados uns dos outros por mesênquima, que forma tecido intersticial composto por células intersticiais ou de Leydig. Os cordões seminíferos (e posteriormente os túbulos) são compostos por células sustentaculares, ou células de Sertoli, e suas paredes são formadas por espermatogônias e células de Sertoli. As células intersticiais ou de Leydig secretam testosterona por volta da oitava semana de desenvolvimento, o que é crucial para a diferenciação sexual masculina dos genitais internos e externos. Quase simultaneamente, as células de Sertoli dos túbulos seminíferos produzem a substância inibidora mülleriana (MIS) ou hormônio antimülleriano (AMH).
A vascularização da crista gonadal é um processo dinâmico. O testículo em desenvolvimento recruta e padroniza a vasculatura por um mecanismo de remodelação, enquanto o ovário em desenvolvimento recruta a vasculatura por angiogênese normal. Nos testículos em desenvolvimento, os vasos mesonéfricos preexistentes se dissociam e formam um aglomerado de células endoteliais que migram e, eventualmente, se estabelecem sob o epitélio celômico da gônada. Ali, as células endoteliais se organizam para formar o vaso celômico, que se estende ao longo do comprimento do testículo em sua margem antimesonéfrica. A formação do vaso celômico é uma das primeiras características do desenvolvimento testicular.
Os testículos começam a descer da cavidade abdominal com apenas dez semanas de desenvolvimento. A descida é auxiliada pelo gubernáculo, uma prega do peritônio aderida ao testículo. A descida dos testículos é concluída entre a 25ª e a 35ª semana de desenvolvimento. [8] [9] [10] A criptorquidia é mais comum em bebês prematuros e com baixo peso ao nascer. Aqueles com criptorquidia têm maior probabilidade de desenvolver tumores testiculares, especialmente tumores de células germinativas.
Os ductos mesonéfricos formam o principal ducto genital do embrião masculino, o ducto deferente, conforme descrito abaixo. As partes restantes dos túbulos excretores formam os ductos eferentes, que tornam a rede testicular contínua com o ducto deferente. Os túbulos seminíferos e os túbulos da rede testicular desembocam nos ductos eferentes. [11] [1]
Ovário
Em um feto com cromossomos XX, as gônadas são inicialmente indiferenciadas e permanecem indiferenciadas por mais tempo do que no desenvolvimento gonadal masculino. Tanto genes autossômicos quanto genes no cromossomo X contribuem para a formação do ovário. Fatores de transcrição específicos do ovário induzem a diferenciação ovariana; estes incluem FOXL2 (fator de transcrição forkhead 2), WNT4 (membro 4 da família de sítios de integração MMTV do tipo wingless), RSPO1 (R-spondina 1) e a via da beta-catenina. [11] Somente recentemente a diferenciação do ovário foi identificada como um processo ativo e complexo. [12] Agora se sabe que a ausência de um gene SRY ativo em um indivíduo com cromossomos masculinos não resultará em diferenciação ovariana, mas em disgenesia gonadal variável. [12]
Um feto cromossomicamente feminino (46 XX) não terá um ovário histologicamente distinto até aproximadamente 10 semanas após a fertilização. [12] Os cordões gonadais crescerão na medula do ovário em desenvolvimento para formar uma rede de canais, a rete ovarii. Tanto os canais quanto os cordões gonadais eventualmente degeneram, deixando aglomerados celulares irregulares na parte medular do ovário. Posteriormente, esses aglomerados celulares irregulares são substituídos por estroma vascular que forma a medula ovariana.
Em contraste com os cordões gonadais, os cordões corticais originam-se do epitélio superficial do ovário em desenvolvimento, crescem no mesênquima subjacente e, eventualmente, abrigam as células germinativas primordiais. As células germinativas primordiais aumentam em número no feto por meio do processo de mitose e, eventualmente, diferenciam-se em ovogônias. [12] As ovogônias não se formam após o nascimento. Na 10ª semana, as ovogônias no centro do ovário entram na prófase meiótica como o primeiro indicador óbvio de diferenciação morfológica ovariana. A maturação do ovário prossegue dessa maneira, do centro para a periferia. [12]
As ovogônias são envolvidas por uma única camada de células foliculares, ou da granulosa. Ao final do sétimo mês de gestação, a atividade mitótica cessa e quase todas as células germinativas entram na prófase I da meiose, sendo interrompidas no estágio de diplóteno — os folículos primordiais abrigam as ovogônias em meiose (o primeiro estágio da foliculogênese). Os folículos primordiais permanecem dormentes até serem estimulados na maturidade sexual para formar folículos primários (o segundo estágio da foliculogênese). [13] Após a maturidade sexual, uma pequena amostra de oócitos primários amadurece mensalmente e completa a primeira divisão meiótica para formar um oócito secundário. O processo que envolve a dormência prolongada e a conclusão da meiose na ovulação é distinto nas mulheres, enquanto a meiose começa na puberdade na gônada masculina.
Outra distinção notável entre o desenvolvimento gonadal masculino e feminino envolve o papel das células germinativas. O desenvolvimento dos testículos fetais não depende de células germinativas, enquanto os folículos ovarianos requerem células germinativas para o seu desenvolvimento. Assim, o envolvimento das células germinativas na estabilização das gônadas é uma das principais diferenças entre o desenvolvimento do ovário e do testículo. A característica da diferenciação testicular é a formação do vaso celômico, que não ocorre no desenvolvimento do ovário. [11] [14] [12]
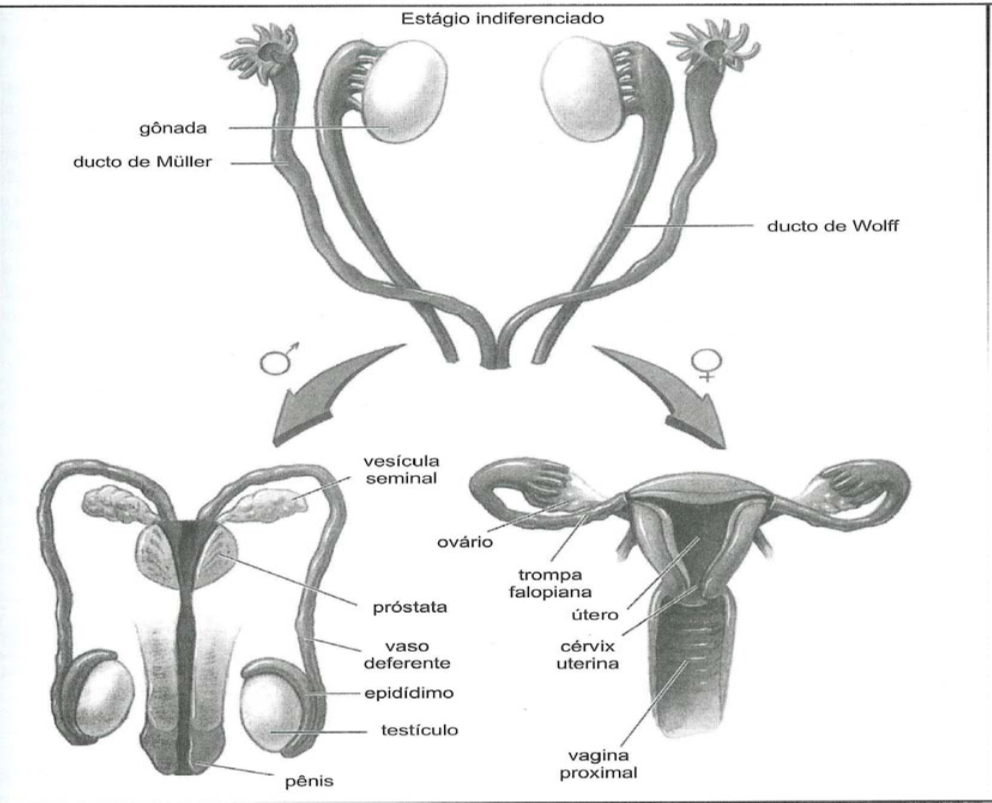
Diferenciação dos órgãos genitais internos
No início do desenvolvimento, tanto os embriões XX quanto os XY possuem dois pares de ductos genitais: os ductos paramesonéfricos (ou ductos de Müller) e os ductos mesonéfricos (ou ductos de Wolff). Ambos os pares de ductos genitais se formam na superfície dos rins mesonéfricos. Por volta de 6 a 7 semanas após a fertilização, os ductos paramesonéfricos se desenvolvem adjacentes aos ductos mesonéfricos. Inicialmente, ambos os pares de ductos são indiferenciados. Na diferenciação sexual da linhagem feminina, os ductos paramesonéfricos ou de Müller desempenham um papel fundamental no desenvolvimento dos órgãos genitais internos femininos. Os ductos de Müller formam as trompas de Falópio (nt.: atualmente se denomina de tubas uterinas), o útero e a porção superior da vagina. Em indivíduos cromossomicamente masculinos, os ductos de Müller geralmente regridem sob a influência da substância inibidora mülleriana derivada dos testículos, também conhecida como hormônio antimülleriano. [15] Nos homens, os ductos de Wolff são essenciais para a formação dos órgãos genitais internos masculinos e produzem o epidídimo, o ducto deferente e a vesícula seminal. A diferenciação masculina dos ductos de Wolff é mediada por andrógenos derivados dos testículos. Nas mulheres, os ductos de Wolff regridem.
Ductos Müllerianos
Os ductos de Müller são os progenitores do trato genital feminino superior e desenvolvem-se inicialmente a partir do mesoderma intermediário. A formação dos ductos de Müller envolve três fases: especificação, invaginação e alongamento. [16] Os ductos de Müller desenvolvem-se inicialmente como uma fenda epitelial celômica na superfície das cristas gonadais, entre 5 e 6 semanas após a fertilização. Por fim, as invaginações celômicas formam as aberturas infundibulares das trompas de Falópio na cavidade peritoneal. Os ductos de Müller, em pares, crescem caudalmente até alcançarem o seio urogenital. Se os ductos de Müller não se fundirem com o seio urogenital, pode ocorrer agenesia vaginal inferior. Por vezes, a falha na formação dos ductos de Müller resulta em agenesia uterina e vaginal em mulheres, levando à amenorreia primária em meninas (síndrome de MRKH). Os ductos de Müller formam as trompas de Falópio (nt.: ou mais modernamente -tubas uterinas-), em suas extremidades craniais e se fundem ao longo da linha média para formar o útero e a parte superior da vagina em suas extremidades caudais.
No início do desenvolvimento fetal de um macho, as células de Sertoli dos testículos começam a secretar o hormônio antimülleriano. Isso é mediado pela beta-catenina, fazendo com que os ductos de Müller regridam em vez de se desenvolverem em órgãos reprodutivos femininos. [15] [16] [17] [18]
Dutos Wolffianos
Os ductos de Wolff, ou inicialmente ductos mesonéfricos, originam-se do mesoderma intermediário. Os ductos mesonéfricos desempenham um papel significativo no desenvolvimento do feto, tanto masculino quanto feminino. Esses ductos induzem a formação de três gerações sucessivas de rins: o pronefro, o mesonefro e o metanefro. Inicialmente, os ductos mesonéfricos drenam o rim de primeira geração, ou pronefro. Posteriormente, durante o desenvolvimento, o ducto mesonéfrico é incorporado e funciona como o ducto excretor do rim de segunda geração, ou mesonefro. Após o desenvolvimento do rim definitivo, os ductos mesonéfricos remanescentes adquirem uma função reprodutiva e são frequentemente denominados ductos de Wolff nesse contexto. [19] [20]
Nos homens, as porções cranianas dos ductos de Wolff persistem e formam o apêndice do epidídimo e a rede testicular. A parte do ducto de Wolff imediatamente inferior a essa área alonga-se e se contorce para formar o epidídimo. O restante do ducto de Wolff desenvolve gradualmente uma espessa camada muscular e forma o ducto deferente. Os ductos de Wolff também produzem as vesículas seminais, que se desenvolvem a partir da extremidade caudal dos ductos como um divertículo lateral. Além disso, uma parte do ducto de Wolff forma o ducto ejaculatório comum entre a vesícula seminal e a uretra.
Durante a 9ª e 10ª semanas após a fertilização, ocorre a diferenciação das células de Leydig induzida pelo SRY, levando à produção de testosterona. A testosterona desempenha um papel importante na estabilização e diferenciação masculina do ducto de Wolff. A testosterona produzida localmente pelos testículos é essencial para a virilização direta dos ductos de Wolff. A ausência de testosterona em fêmeas, e em alguns machos, leva à regressão do ducto de Wolff durante a diferenciação sexual. [21] [22] [23]
Diferenciação dos Genitais Externos
Assim como as gônadas e os órgãos genitais internos, os órgãos genitais externos são indiferenciados no início do desenvolvimento. Na 5ª semana, células mesenquimais migram para o períneo para formar protuberâncias em ambos os lados da cloaca, chamadas pregas cloacais. Na porção cranial das pregas cloacais, as células mesenquimais se fundem ao longo da linha média para formar o tubérculo genital. O tubérculo genital está localizado logo acima do óstio urogenital e é o primórdio do futuro clitóris ou pênis em desenvolvimento. Logo após o desenvolvimento do tubérculo genital, formam-se as pregas urogenitais e labioscrotais lateralmente à membrana cloacal. Esses estágios são idênticos em fetos cromossomicamente masculinos e femininos, e permanecem idênticos até aproximadamente a 9ª semana pós-fertilização. [8] Nesse ponto, o tubérculo genital sofre alongamento e diferenciação sexual ao longo do caminho que leva ao pênis masculino primordial ou ao clitóris feminino primordial.
Genitália externa masculina
Nos embriões masculinos, a masculinização dos genitais externos in utero ocorre em resposta à diidrotestosterona (DHT). [20] A testosterona secretada pelas células de Leydig é convertida em DHT pela 5-alfa-redutase. Em resposta, o tubérculo genital sofre crescimento e alongamento para formar o pênis — o escroto se forma pela fusão das pregas labioscrotais na linha média. Mais tarde no desenvolvimento, o local de fusão é demarcado pela rafe escrotal. Uma placa epitelial sólida, ou uretral, se forma na superfície ventral do pênis em desenvolvimento. A placa epitelial sofre canalização, formando primeiro um sulco na superfície do tubérculo genital, que é delimitado pelas pregas uretrais. Em seguida, as pregas uretrais se fundem ao longo da linha média e convertem o sulco uretral em uma uretra peniana totalmente contida, onde o local de fusão do ectoderma superficial é demarcado pela rafe peniana. A falha nesse processo pode resultar na formação de hipospádia devido à insuficiência de andrógenos durante esse período crítico de desenvolvimento. Hipospádia é uma localização anormal do meato uretral externo em algum ponto da superfície ventral do pênis e recebe o nome de acordo com sua localização: glandular, coronal, peniana ou perineal.
A glande forma um cordão ectodérmico que se estende proximalmente até se tornar contínuo com a uretra esponjosa. O prepúcio peniano se forma por volta da 12ª semana após a fertilização, devido ao crescimento de ectoderma próximo à margem da glande, que posteriormente se desprende. O desenvolvimento dos genitais externos masculinos geralmente se completa por volta da 14ª semana de gestação.
Genitália externa feminina
O desenvolvimento dos genitais externos femininos é regulado pela ausência de andrógenos e pela presença de estrogênios maternos. Na ausência de testosterona, o tubérculo genital se expande para formar o clitóris, mas a uma taxa relativamente mais lenta do que a expansão do tubérculo genital nos homens. O desenvolvimento dos genitais externos femininos difere do masculino pelo fato de as pregas urogenitais e labioscrotais permanecerem em grande parte não fundidas. As pregas urogenitais se fundem ao longo de sua margem posterior para formar o frênulo do clitóris, enquanto as porções não fundidas das pregas urogenitais formam os pequenos lábios. As pregas labioscrotais se fundem anteriormente para produzir a comissura labial anterior e o monte púbico, e se fundem posteriormente para formar a comissura labial posterior. No entanto, a maior parte das pregas labioscrotais permanece não fundida e, por fim, forma os grandes lábios.
O desenvolvimento vaginal envolve tanto os ductos de Müller quanto o seio urogenital. A extremidade caudal dos ductos de Müller fundidos forma o primórdio uterovaginal, que entra em contato com a parte posterior do seio urogenital. Esse processo resulta na formação do tubérculo sinusal, que induz o surgimento de projeções endodérmicas pareadas para formar os bulbos sinovaginais. Os bulbos sinovaginais conectam o seio urogenital ao primórdio uterovaginal. Os bulbos sinovaginais se fundem para formar uma placa vaginal sólida que, posteriormente, forma um lúmen aberto. Os bulbos sinovaginais dão origem aos dois terços inferiores do canal vaginal. O hímen é formado durante o desenvolvimento uterovaginal como um revestimento que separa o canal vaginal do seio urogenital.
O epitélio da vagina é derivado do endoderma, enquanto as paredes musculares da vagina são derivadas do mesênquima. A diferenciação dos genitais externos femininos começa às 11 semanas e completa-se às 20 semanas após a fertilização. [8]
Significado clínico
O exame cuidadoso de um recém-nascido é crucial e inclui a avaliação da simetria e pigmentação dos genitais externos, presença de gônadas palpáveis e morfologia labioscrotal. Além disso, a medida do pênis deve ser registrada, e a posição do meato uretral e o número de óstios perineais avaliados. Após o nascimento, a determinação do sexo biológico é uma importante decisão clínica. O sexo biológico é frequentemente atribuído no momento do nascimento com base na aparência dos genitais externos. O exame dos genitais externos é a maneira mais simples de determinar o sexo após o nascimento, mas é menos confiável do que a avaliação genética. Os genitais externos são altamente suscetíveis a variações decorrentes da diferenciação sexual ao longo de uma trajetória tipicamente masculina ou tipicamente feminina e podem apresentar algum grau de genitália ambígua. Recém-nascidos que apresentam qualquer grau de genitália ambígua tendem a representar um desafio para os médicos que cuidam deles e causam angústia aos pais. [12]
As diferenças no desenvolvimento sexual (DDS), anteriormente conhecidas como distúrbios do desenvolvimento sexual ou condições intersexuais, são um grupo de condições associadas ao desenvolvimento atípico das gônadas, genitália interna ou genitália externa. Em alguns indivíduos, há um conflito entre o sexo cromossômico e a diferenciação sexual das gônadas, genitália externa, genitália interna ou características sexuais secundárias (posteriores). As DDS são, por vezes, identificadas in utero devido à avaliação genética de rotina, ao nascimento devido à presença de genitália ambígua ou, por vezes, muito tempo após o nascimento devido à virilização, puberdade tardia ou infertilidade. [12] Os pacientes com essas condições enfrentam estigma que impacta negativamente sua saúde psicossocial.
As diferenças no desenvolvimento sexual podem ser organizadas em esquemas de classificação abrangentes. Existem inúmeras condições classificadas como DSDs; algumas das mais comuns ou mais bem compreendidas incluem: [24] [12]
46 XX DSD
Este grupo de condições de DSD afeta indivíduos com cromossomos sexuais XX que apresentam desenvolvimento atípico das gônadas, genitália interna, genitália externa e/ou características sexuais secundárias. Algumas dessas condições incluem:
Desenvolvimento ovariano aberrante
Excesso de andrógenos
- Deficiência fetal (de 21- ou 11-hidroxilase)
- Fetoplacentário (deficiência de aromatase)
- Materno (luteoma, exógeno)
46 XY DSD
Este grupo de condições de DSD afeta indivíduos com cromossomos sexuais XY que apresentam desenvolvimento atípico das gônadas, genitália interna, genitália externa e/ou características sexuais secundárias. Algumas dessas condições incluem:
Desenvolvimento testicular anormal
- Disgenesia gonadal completa e parcial
- Regressão gonadal
Defeitos na biossíntese de andrógenos
- Deficiência de 17-hidroxiesteroide desidrogenase
- deficiência de 5-alfa redutase
Defeitos na ação dos andrógenos
- Síndrome de insensibilidade aos andrógenos (completa ou parcial)
Distúrbios do AMH e do receptor de AMH
- Síndrome do ducto de Müller persistente
Defeito do receptor LH
- Hipoplasia das células de Leydig
Outras (hipospádia e extrofia cloacal)
DSD dos Cromossomos Sexuais
Este grupo de condições de DSD afeta indivíduos com cromossomos sexuais atípicos, resultando em uma série de possíveis alterações no desenvolvimento. Algumas dessas condições incluem:
45 X (Síndrome de Turner e suas variantes)
47 XXY (Síndrome de Klinefelter e suas variantes)
DSD ovotesticular
Discussão
A hiperplasia adrenal congênita (HAC) é uma causa comum de distúrbios do desenvolvimento sexual 46,XX (DDS 46,XX) resultantes do excesso de andrógenos. Trata-se de um grupo de distúrbios que afetam o desenvolvimento das glândulas adrenais e podem envolver diversos efeitos metabólicos. Na maioria dos indivíduos com essa condição, há deficiência da enzima 21-hidroxilase, o que resulta em deficiência de mineralocorticoides e formação excessiva de produtos androgênicos. Essa condição causa virilização excessiva em indivíduos com cromossomos sexuais XX. A apresentação clínica depende da gravidade do excesso de andrógenos e do momento do desenvolvimento.
A síndrome de insensibilidade aos andrógenos (SIA), ou insensibilidade completa aos andrógenos, é uma condição na qual uma pessoa com cromossomos sexuais XY não responde aos andrógenos. Indivíduos com essa condição, embora cromossomicamente masculinos, apresentam-se ao nascer e durante o desenvolvimento como mulheres, com características psicosexuais tipicamente femininas e, frequentemente, são criados como mulheres. Esses indivíduos possuem genitália externa feminina típica, mas não têm útero e, portanto, são inférteis.
A insensibilidade parcial aos andrógenos é uma condição semelhante à do cariótipo 46,XY, que envolve morfologia submasculinizada. Indivíduos com síndrome de insensibilidade parcial aos andrógenos podem apresentar genitália externa feminina levemente virilizada (clitoromegalia) ou genitália externa masculina levemente subvirilizada (hipospádia e/ou micropênis). Em ambos os casos, os indivíduos afetados possuem testículos e tipicamente apresentam produção normal de testosterona e DHT.
A deficiência da enzima 5-alfa-redutase tipo 2, uma DSD autossômica recessiva 46,XY, resulta de uma mutação no gene SRD5A2. Essa enzima converte a testosterona em DHT, responsável pela masculinização dos genitais externos no útero . Recém-nascidos com deficiência de 5-alfa-redutase apresentam graus variáveis de genitália ambígua, como falo semelhante ao clitóris, escroto bífido e hipospádia perineoscrotal pseudovaginal. Na puberdade, como a masculinização nesse período envolve outros andrógenos, o indivíduo afetado pode apresentar genitália externa progressivamente virilizada.
Hipospádia é um exemplo de uma condição comum associada à DSD 46,XY, que envolve um meato uretral externo ectópico na face ventral do pênis. Dependendo da localização do meato uretral externo, a hipospádia pode ser assintomática ou causar outros problemas. Por exemplo, a hipospádia granular pode ser um achado incidental, enquanto a hipospádia peniana ou perineal pode estar associada a jato urinário anormal, curvatura peniana anormal (corda peniana) ou infertilidade por meio de relações sexuais. A epispádia se distingue da hipospádia por tender a ocorrer muito mais cedo no desenvolvimento e se apresentar como uma abertura anormal do meato uretral externo na face dorsal do pênis.
As DSDs dos cromossomos sexuais incluem condições como a síndrome de Turner e a síndrome de Klinefelter. A incidência da síndrome de Turner é de aproximadamente 1 em 2500 meninas nascidas vivas. A síndrome de Turner é frequentemente diagnosticável ao nascimento devido a características como baixo peso ao nascer, linfedema nas mãos e nos pés e pescoço curto. No entanto, outras formas da síndrome de Turner podem se manifestar mais tarde com baixa estatura e atraso na puberdade. Alguns cariótipos da síndrome de Turner incluem 45 XO, 45 XO/46 XX ou 45 XO/46 XY. A síndrome de Klinefelter é outra DSD dos cromossomos sexuais que ocorre em 1 em cada 1000 meninos nascidos vivos. As características clínicas dos indivíduos afetados incluem estatura alta, fraqueza muscular, testículos pequenos, ginecomastia, puberdade tardia e infertilidade. [24] [25] [26] [27]
Referências
1.Pask A. The Reproductive System. Adv Exp Med Biol. 2016;886:1-12. [PubMed]
2.She ZY, Yang WX. Molecular mechanisms involved in mammalian primary sex determination. J Mol Endocrinol. 2014 Aug;53(1):R21-37. [PubMed]
3.Makiyan Z. Studies of gonadal sex differentiation. Organogenesis. 2016 Jan 02;12(1):42-51. [PMC free article] [PubMed]
4.Biason-Lauber A. The Battle of the Sexes: Human Sex Development and Its Disorders. Results Probl Cell Differ. 2016;58:337-82. [PubMed]
5.Gunes SO, Metin Mahmutoglu A, Agarwal A. Genetic and epigenetic effects in sex determination. Birth Defects Res C Embryo Today. 2016 Dec;108(4):321-336. [PubMed]
6.Eid W, Biason-Lauber A. Why boys will be boys and girls will be girls: Human sex development and its defects. Birth Defects Res C Embryo Today. 2016 Dec;108(4):365-379. [PubMed]
7.Agrawal R, Wessely O, Anand A, Singh L, Aggarwal RK. Male-specific expression of Sox9 during gonad development of crocodile and mouse is mediated by alternative splicing of its proline-glutamine-alanine rich domain. FEBS J. 2009 Aug;276(15):4184-96. [PubMed]
8.Blaschko SD, Cunha GR, Baskin LS. Molecular mechanisms of external genitalia development. Differentiation. 2012 Oct;84(3):261-8. [PMC free article] [PubMed]
9.Baskin LS. Hypospadias and urethral development. J Urol. 2000 Mar;163(3):951-6. [PubMed]
10.Cunha GR, Baskin LS. Development of the external genitalia. Differentiation. 2020 Mar-Apr;112:7-9. [PMC free article] [PubMed]
11.Ray R, Racine C. Sexual Differentiation. In: Feingold KR, Adler RA, Ahmed SF, Anawalt B, Blackman MR, Chrousos G, Corpas E, de Herder WW, Dhatariya K, Dungan K, Hamilton E, Hofland J, Jan de Beur S, Kalra S, Kaltsas G, Kapoor N, Kim M, Koch C, Kopp P, Korbonits M, Kovacs CS, Kuohung W, Laferrère B, Levy M, McGee EA, McLachlan R, Muzumdar R, Purnell J, Rey R, Sahay R, Shah AS, Sperling MA, Stratakis CA, Trence DL, Wilson DP, editors. Endotext [Internet]. MDText.com, Inc.; South Dartmouth (MA): Jul 24, 2025. [PubMed]
12.Witchel SF. Disorders of sex development. Best Pract Res Clin Obstet Gynaecol. 2018 Apr;48:90-102. [PMC free article] [PubMed]
13.Fortune JE, Cushman RA, Wahl CM, Kito S. The primordial to primary follicle transition. Mol Cell Endocrinol. 2000 May 25;163(1-2):53-60. [PubMed]
14.Richards JS, Ren YA, Candelaria N, Adams JE, Rajkovic A. Ovarian Follicular Theca Cell Recruitment, Differentiation, and Impact on Fertility: 2017 Update. Endocr Rev. 2018 Feb 01;39(1):1-20. [PMC free article] [PubMed]
15.Roly ZY, Backhouse B, Cutting A, Tan TY, Sinclair AH, Ayers KL, Major AT, Smith CA. The cell biology and molecular genetics of Müllerian duct development. Wiley Interdiscip Rev Dev Biol. 2018 May;7(3):e310. [PubMed]
16.Mullen RD, Behringer RR. Molecular genetics of Müllerian duct formation, regression and differentiation. Sex Dev. 2014;8(5):281-96. [PMC free article] [PubMed]17.
Arango NA, Kobayashi A, Wang Y, Jamin SP, Lee HH, Orvis GD, Behringer RR. A mesenchymal perspective of Müllerian duct differentiation and regression in Amhr2-lacZ mice. Mol Reprod Dev. 2008 Jul;75(7):1154-62. [PubMed]
18.Cunha GR, Robboy SJ, Kurita T, Isaacson D, Shen J, Cao M, Baskin LS. Development of the human female reproductive tract. Differentiation. 2018 Sep-Oct;103:46-65. [PMC free article] [PubMed]
19.Shaw G, Renfree MB. Wolffian duct development. Sex Dev. 2014;8(5):273-80. [PubMed]
20.Sajjad Y. Development of the genital ducts and external genitalia in the early human embryo. J Obstet Gynaecol Res. 2010 Oct;36(5):929-37. [PubMed]
21.Patel N, Zafar Gondal A. StatPearls [Internet]. StatPearls Publishing; Treasure Island (FL): Aug 14, 2023. Embryology, Mullerian-inhibiting Factor. [PubMed]
22.Murashima A, Xu B, Hinton BT. Understanding normal and abnormal development of the Wolffian/epididymal duct by using transgenic mice. Asian J Androl. 2015 Sep-Oct;17(5):749-55. [PMC free article] [PubMed]
23.Sekido R, Bar I, Narváez V, Penny G, Lovell-Badge R. SOX9 is up-regulated by the transient expression of SRY specifically in Sertoli cell precursors. Dev Biol. 2004 Oct 15;274(2):271-9. [PubMed]
24.Kim KS, Kim J. Disorders of sex development. Korean J Urol. 2012 Jan;53(1):1-8. [PMC free article] [PubMed]
25.Fisher AD, Ristori J, Fanni E, Castellini G, Forti G, Maggi M. Gender identity, gender assignment and reassignment in individuals with disorders of sex development: a major of dilemma. J Endocrinol Invest. 2016 Nov;39(11):1207-1224. [PubMed]
26.Ernst MM, Liao LM, Baratz AB, Sandberg DE. Disorders of Sex Development/Intersex: Gaps in Psychosocial Care for Children. Pediatrics. 2018 Aug;142(2) [PMC free article] [PubMed]
27.Lee PA, Nordenström A, Houk CP, Ahmed SF, Auchus R, Baratz A, Baratz Dalke K, Liao LM, Lin-Su K, Looijenga LH, Mazur T, Meyer-Bahlburg HF, Mouriquand P, Quigley CA, Sandberg DE, Vilain E, Witchel S., Global DSD Update Consortium. Global Disorders of Sex Development Update since 2006: Perceptions, Approach and Care. Horm Res Paediatr. 2016;85(3):158-80. [PubMed]
Declaração: A Aatsha PA declara não possuir relações financeiras relevantes com empresas inelegíveis.
Declaração: A Tafline Arbor declara não possuir relações financeiras relevantes com empresas inelegíveis.
Declaração: Kewal Krishan declara não possuir relações financeiras relevantes com empresas inelegíveis.
Direitos autorais © 2026, StatPearls Publishing LLC.
Tradução livre, parcial, de Luiz Jacques Saldanha, maio de 2026

