https://academic.oup.com/humupd/article/29/2/157/6824414
Hagai Levine, Niels Jørgensen, Anderson Martino-Andrade, Jaime Mendiola, Dan Weksler-Derri, Maya Jolles, Raquel Pinotti, e Shanna H Swan
Human Reproduction Update, Volume 29, Issue 2, March-April 2023
[NOTA DO WEBSITE 1: Sem comentários! Desde 1989, todos nós, da humanidade, passamos a saber que algo estava comprometendo a saúde dos homens. E pior, também por tecnologias ‘modernas’, como plásticos e agrotóxicos, primeira e principalmente desenvolvidas por homens. Os resultados e a realidade estão postos. DEVEMOS LEMBRAR QUE OS JOVENS HOMENS DE HOJE FORAM GESTADOS EM ÚTEROS DE MÃES QUE ESTAVAM CONTAMINADAS. Ou seja, os fetos foram formados com a contribuição dessas moléculas e se desenvolveram num ambiente em que todas elas estavam em seus cotidianos. AGORA IMAGINA-SE COMO DEVEM ESTAR OS BEBÊS, AS CRIANÇAS E OS ADOLESCENTES QUE VIERAM DEPOIS DE SEUS JOVENS PAIS?].
[NOTA DO WEBSITE 2: como esse trabalho científico é muito extenso, além de conter informações por demais técnicas para pessoas como nós, fizemos uma compilação inicial com os dados que realmente nos interessam direta e objetivamente. Abaixo, estará a pesquisa em sua totalidade para os que se interessarem por seu conhecimento completo].
Uma revisão sistemática e análise de meta-regressão de amostras coletadas globalmente nos séculos XX e XXI.
SINOPSE FEITA PELO WEBSITE – dados e informações que nos darão condições de compreensão do valor da profundidade da pesquisa.
Numerosos estudos relataram declínios na qualidade do sêmen e outros marcadores da saúde reprodutiva masculina. Nossa metanálise anterior relatou uma diminuição significativa na concentração de espermatozoides (SC/sperm concentration) e na contagem total de espermatozoides (TSC/total sperm count) entre homens da América do Norte-Europa-Austrália. O objetivo deste estudo foi examinar as tendências na contagem de espermatozoides entre homens de todos os continentes, incluindo Américas do Sul e Central, além da Ásia e África.
No geral, a SC diminuiu sensivelmente entre 1973 e 2018. Entre os homens não selecionados de todos os continentes, a SC média diminuiu 51,6% entre 1973 e 2018. A inclinação para SC entre homens não selecionados foi mais acentuada em um modelo restrito a dados pós-2000 e o declínio percentual por ano dobrou, aumentando de 1,16% pós-1972 para 2,64%. pós-2000. Os resultados foram semelhantes para o TSC, com um declínio global de 62,3% entre os homens não selecionados. (nt.: destacamos esse parágrafo porque ele nos dá a situação real nesse momento histórico da humanidade!)
Além disso, os dados sugerem que este declínio mundial continua no século XXI a um ritmo acelerado. São urgentemente necessárias pesquisas sobre as causas deste declínio contínuo e ações para prevenir novas perturbações na saúde reprodutiva masculina.
Resumo gráfico
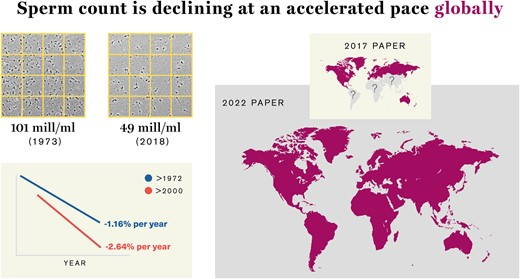
O reconhecimento da importância da função reprodutiva masculina e da contagem de espermatozoides aumentou desde 2017.
O fardo econômico e social da infertilidade masculina é agora amplamente reconhecido, tal como o fardo desigual da infertilidade masculina, que recai mais pesadamente sobre as populações de baixos rendimentos. Evidências cada vez mais fortes ligam a redução da contagem e concentração de espermatozoides ao aumento da mortalidade e morbidade por todas as causas. As ligações entre a contagem de espermatozoides e a infertilidade são bem reconhecidas. Além disso, o declínio na contagem de espermatozoides é acompanhado por declínios na testosterona e aumentos no câncer testicular e anomalias genitais masculinas. Na verdade, o declínio na qualidade do sêmen e na saúde reprodutiva masculina foi recentemente descrito como uma crise.
Discussão
Os resultados do presente estudo ampliam os da nossa metanálise de 2017. Conforme detalhado abaixo, os novos dados permitem novas análises e novos resultados. Fornecemos fortes evidências, pela primeira vez, de um declínio na contagem de espermatozoides entre homens da América do Sul/Central, Ásia e África, bem como de um declínio mundial no século XXI, com dados que sugerem que o ritmo deste o declínio acelerou.
Principais conclusões
O que há de novo em a análise atual?
Nossa análise atual, a maior já realizada a examinar tendências temporais na contagem de espermatozoides, amplia tanto o período de estudo quanto o número de estimativas.
A distribuição dos países contribuintes mudou desde a nossa análise de 2017. Esta análise fornece fortes evidências, pela primeira vez, de um declínio apreciável na contagem de espermatozoides entre homens. É importante ressaltar que esta análise também demonstra um declínio acelerado na SC e na TSC pós-2000. Em resumo, esta atualização confirma, amplia e fortalece os resultados da nossa análise de 2017.
Conclusão e implicações mais amplas
Os nossos novos dados e análises confirmam as nossas descobertas anteriores de um declínio apreciável na contagem de espermatozoides entre 1973 e 2018 entre homens da América do Norte, Europa e Austrália e apoiam um declínio entre homens não selecionados da América do Sul/Central, África e Ásia. Este declínio continuou, conforme previsto pela nossa análise anterior, e tornou-se mais acentuado desde 2000. Este declínio substancial e persistente é agora reconhecido como um problema significativo de saúde pública. Em 2018, um grupo de médicos e cientistas líderes apelou aos governos para que reconhecessem a diminuição da fertilidade masculina como um importante problema de saúde pública e para que reconhecessem a importância da saúde reprodutiva masculina para a sobrevivência da espécie humana (e de outras) (Levine et al., 2018). São necessárias pesquisas sobre as causas deste declínio contínuo e uma resposta imediata e focada para evitar maiores perturbações na saúde reprodutiva masculina.
Esperamos que as novas evidências aqui fornecidas recebam a atenção não só dos médicos e cientistas, mas também daqueles que tomam decisões públicas e da população em geral.
[NOTA DO WEBSITE: a partir desse ponto, está a completude da pesquisa, sem a nominata da bibliografia por não termos sabido fazer a transposição da publicação original do trabalho para nosso website. A transposição ficou completamente desformatada].
RESUMO – RETROSPECTIVA
Numerosos estudos relataram declínios na qualidade do sêmen e outros marcadores da saúde reprodutiva masculina. Nossa metanálise anterior relatou uma diminuição significativa na concentração de espermatozoides (SC/sperm concentration) e na contagem total de espermatozoides (TSC/total sperm count) entre homens da América do Norte-Europa-Austrália (NEA/North America–Europe–Australia) com base em estudos publicados durante 1981-2013. Naquela altura, havia poucos estudos com dados da América do Sul/Central–Ásia–África (SAA/South/Central America–Asia–Africa) para estimar de forma confiável as tendências entre os homens destes continentes.
OBJETIVO E JUSTIFICATIVA
O objetivo deste estudo foi examinar as tendências na contagem de espermatozoides entre homens de todos os continentes. As implicações mais amplas de um declínio global na contagem de espermatozoides, as lacunas de conhecimento deixadas por preencher pela nossa análise anterior e as controvérsias em torno desta questão justificaram uma meta-análise atualizada.
MÉTODOS DE PESQUISA
Pesquisamos na PubMed/MEDLINE e EMBASE para identificar estudos de SC e TSC humanos publicados durante 2014–2019. Após revisão de 2.936 resumos e 868 artigos completos, 44 estimativas de SC e TSC de 38 estudos atenderam aos critérios do protocolo. Foram extraídos dados sobre parâmetros do sêmen (SC, TSC, volume de sêmen), ano de coleta e covariáveis. Combinando estes novos dados com os dados da nossa metanálise anterior, a atual inclui resultados de 223 estudos, produzindo 288 estimativas baseadas em amostras de sémen recolhidas entre 1973 e 2018. As inclinações das SC e TSC foram estimadas em função do ano de coleta da amostra usando regressão linear simples, bem como meta-regressão ponderada. Os últimos modelos foram ajustados para covariáveis predeterminadas e examinados quanto à modificação pelo status de fertilidade (não selecionado por fertilidade versus fértil) e por dois grupos de continentes: NEA e SAA. Estas análises foram repetidas para dados recolhidos após 2000. Foram realizadas múltiplas análises de sensibilidade para examinar suposições, incluindo a linearidade.
RESULTADOS
No geral, a SC diminuiu sensivelmente entre 1973 e 2018 (inclinação no modelo linear simples: –0,87 milhões/ml/ano, IC 95%: –0,89 a –0,86; P < 0,001). Em um modelo de meta-regressão ajustado, que incluiu dois termos de interação [tempo × grupo de fertilidade (P = 0,012) e tempo × continentes (P = 0,058)], foram observados declínios entre homens não selecionados do NEA (–1,27; –1,78 a – 0,77; P < 0,001) e homens não selecionados da SAA (–0,65; –1,29 a –0,01; P = 0,045) e homens férteis da NEA (–0,50; –1,00 a –0,01; P = 0,046). Entre os homens não selecionados de todos os continentes, a SC média diminuiu 51,6% entre 1973 e 2018 (–1,17: –1,66 a –0,68; P < 0,001). A inclinação para SC entre homens não selecionados foi mais acentuada em um modelo restrito a dados pós-2000 (–1,73: –3,23 a –0,24; P = 0,024) e o declínio percentual por ano dobrou, aumentando de 1,16% pós-1972 para 2,64%. pós-2000. Os resultados foram semelhantes para o TSC, com um declínio global de 62,3% entre os homens não selecionados (–4,70 milhões/ano; –6,56 a –2,83; P < 0,001) no modelo de meta-regressão ajustado. Todos os resultados mudaram apenas minimamente em análises de sensibilidade múltipla.
IMPLICAÇÕES MAIS AMPLAS
Esta análise é a primeira a relatar um declínio na contagem de espermatozoides entre homens não selecionados da América do Sul/Central-Ásia-África, em contraste com a nossa metanálise anterior, que não tinha poder suficiente para examinar esses continentes. Além disso, os dados sugerem que este declínio mundial continua no século XXI a um ritmo acelerado. São urgentemente necessárias pesquisas sobre as causas deste declínio contínuo e ações para prevenir novas perturbações na saúde reprodutiva masculina.
Resumo gráfico
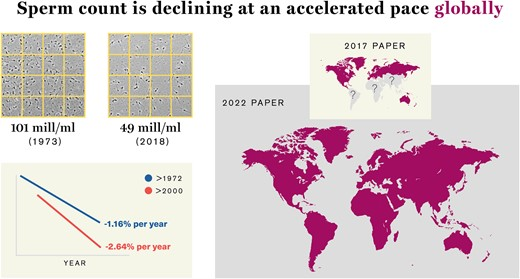
A contagem de espermatozoides está diminuindo em ritmo acelerado, em todo o mundo.
Abrir em nova aba Baixar slide
Introdução
Em 2017, ‘Tendências temporais na contagem de esperma: uma revisão sistemática e análise de meta-regressão’ foi publicado por esta revista (Levine et al. , 2017). Esse artigo, que foi amplamente discutido e altamente citado, inclui todas as publicações elegíveis em língua inglesa em 1981–2013 que continham dados sobre a contagem de espermatozoides. Relatamos um declínio muito forte na concentração de espermatozoides (SC) e na contagem total de espermatozoides (TSC) na América do Norte, Europa, Austrália/Nova Zelândia (doravante NEA), mas poucos estudos foram publicados na América do Sul/Central, Ásia e África ( doravante SAA) para tirar uma conclusão sobre as tendências nesses continentes. Examinamos as médias de SC e TSC em função do ano de coleta, aproximado pelo meio do ano do período de coleta da amostra. Como a coleta da amostra precedeu o ano de publicação em uma média de 6 anos, nossos resultados já estavam um tanto desatualizados quando publicamos nossa análise em 2017. Portanto, conduzimos uma nova pesquisa bibliográfica na primavera de 2020 para identificar estudos elegíveis publicados entre 1º de janeiro de 2014 e 31 de dezembro de 2019. Aqui, relatamos as tendências globais em SC e TSC em publicações de 1981 a 2019, que combina resultados de pesquisas e análises . Esta análise ampliada aborda duas questões importantes. Com o aumento do tamanho da amostra, foi observada uma tendência na América do Sul, África e Ásia? As tendências que relatamos continuaram após 2011?
O reconhecimento da importância da função reprodutiva masculina e da contagem de espermatozoides aumentou desde 2017 (Levine et al. , 2018 ; Gabinete do Alto Comissariado das Nações Unidas para os Direitos Humanos, 2019). O fardo econômico e social da infertilidade masculina é agora amplamente reconhecido, tal como o fardo desigual da infertilidade masculina, que recai mais pesadamente sobre as populações de baixos rendimentos (Winters e Walsh, 2014 ; Hauser et al., 2015; Dupree, 2016; Skakkebaek et al., 2015; Dupree, 2016 ; Skakkebaek et al. al. , 2016). Evidências cada vez mais fortes ligam a redução da contagem e concentração de espermatozoides ao aumento da mortalidade e morbidade por todas as causas (Latife outros, 2017 ; Del Giudice e cols., 2021 ; Ferlin et al., 2021). As ligações entre a contagem de espermatozoides e a infertilidade são bem reconhecidas (Bonde et al., 1998 ; Skakkebæk et al., 2022). Além disso, o declínio na contagem de espermatozoides é acompanhado por declínios na testosterona e aumentos no câncer testicular e anomalias genitais masculinas (Skakkebæk et al., 2022 – https://pubmed.ncbi.nlm.nih.gov/34912078/). Na verdade, o declínio na qualidade do sêmen e na saúde reprodutiva masculina foi recentemente descrito como uma crise (De Jonge e Barratt, 2019). Em relação aos declínios na contagem de espermatozoides, estas últimas tendências são muito mais difíceis de documentar. Atualmente não existe uma coleta sistemática de tais dados, o que torna difícil a análise dessas tendências. Portanto, um grupo internacional de cientistas, incluindo vários dos autores, sugeriu a formação de um sistema de monitorização multidisciplinar para indicadores de saúde reprodutiva que proporcionaria uma vigilância contínua dos resultados da saúde reprodutiva (Le Moal et al. , 2016 ).
As amplas implicações de um declínio global na contagem de espermatozoides, as lacunas de dados deixadas por preencher pela nossa análise anterior e as controvérsias em torno destas questões justificam uma metanálise atualizada. E assim essa metanálise foi conduzida para abordar esses objetivos.
Métodos
Esta revisão sistemática e análise de meta-regressão foram conduzidas, e os resultados relatados, de acordo com Meta-análise em Estudos Observacionais em Epidemiologia ( Stroup et al. , 2000 ) (Tabela Suplementar SI ) e Itens de Relatório Preferenciais para Revisões Sistemáticas e Diretrizes de Meta-Análise ( Liberati et al. , 2009 ; Moher et al. , 2009 ). Nossa equipe de pesquisa incluiu epidemiologistas, andrologistas e um bibliotecário médico. Nosso protocolo predefinido foi desenvolvido seguindo as melhores práticas ( Borenstein et al. , 2009 ; Higgins e Green 2011 ; Programa Nacional de Toxicologia 2015 ) e informado por nosso estudo anterior. Ao longo de todo o processo, salvo indicação em contrário, os métodos do estudo atual são aqueles empregados e publicados no estudo anterior ( Levine et al. , 2017), incluindo palavras-chave e bases de dados pesquisadas, critérios de elegibilidade e métodos estatísticos.
Revisão sistemática e seleção de estudos
Foi realizada uma pesquisa abrangente no PubMed/MEDLINE e EMBASE para identificar publicações em inglês que relatassem dados primários sobre contagem de espermatozoides humanos, publicados em 2014–2019, ou seja, a partir da última data incluída em nossa pesquisa anterior até 2019. Em 15 de maio Em 2020, pesquisamos na MEDLINE/PubMed e na EMBASE/Excerpta Medica database (base de dados Excerpta Medica) publicações revisadas por pares que atendessem aos nossos critérios de inclusão. Seguindo a recomendação do Cochrane Handbook for Systematic Reviews, pesquisamos no título e no resumo termos de índice (MeSH) e palavras-chave e filtramos estudos somente com animais. Usamos o termo MeSH ‘contagem de espermatozoides’, que inclui sete termos adicionais, e para aumentar a sensibilidade, adicionamos 13 palavras-chave relacionadas (por exemplo, ‘densidade do espermatozoide’, ‘concentração de espermatozoides’).
Todos os estudos em inglês que relataram dados primários sobre SC humana foram considerados elegíveis para triagem de resumos. Avaliamos a elegibilidade de todos os subgrupos de um estudo. Por exemplo, num estudo de caso-controle, o grupo controle poderia ter sido elegível para inclusão, embora, com base nos nossos critérios de exclusão, o grupo de caso não o fosse.
Dividimos os estudos elegíveis em dois grupos definidos sobre fertilidade: (i) estudos de homens não selecionados por status de fertilidade, doravante ‘Não selecionados’ (por exemplo, homens jovens que provavelmente não terão conhecimento de sua fertilidade, como homens jovens sendo selecionados para o serviço militar ou estudantes universitários) e (ii) estudos de homens cujas parceiras tiveram um filho ou cujas parceiras estavam grávidas independentemente do resultado da gravidez, doravante ‘Férteis’. ‘Total’ refere-se a ambos os grupos.
Um estudo era excluído se os participantes fossem selecionados com base em: (i) infertilidade ou subfertilidade; (ii) a sua gama de parâmetros de sêmen (por exemplo, estudos que selecionam homens normospérmicos); e (iii) anomalias genitais, doenças ou medicamentos. Também excluímos estudos limitados a homens com exposições que possam afetar a fertilidade, como exposição ocupacional, intervenção pós-ensaio clínico ou tabagismo. Estudos de candidatos à vasectomia ou doação de sêmen foram incluídos apenas se a qualidade do sêmen não fosse um critério para a participação dos homens no estudo. Foram excluídos estudos que utilizaram métodos não padronizados para coleta de espermatozoides (por exemplo, métodos diferentes da masturbação) ou métodos de contagem diferentes do hemocitômetro e estudos com menos de 10 homens.
Primeiro, a publicação foi excluída ou avançada para triagem de texto completo com base no título e no resumo. Qualquer publicação sem resumo foi automaticamente encaminhada para triagem de texto completo. Segundo, revisamos o texto completo e o atribuímos à exclusão (e categorizamos o motivo da exclusão) ou à extração de dados. Em seguida, confirmamos a elegibilidade do estudo e identificamos múltiplas publicações do mesmo estudo para garantir que as estimativas da mesma população não fossem usadas mais de uma vez.
Extração de dados
Para cada estimativa, extraímos estatísticas resumidas sobre SC e TSC (média, desvio padrão, mínimo, máximo, mediana e percentis), volume de sêmen (método médio e medido), tamanho da amostra, anos de coleta de amostra, dados sobre covariáveis (grupo de fertilidade, país, idade, tempo de abstinência ejaculatória relatado e por protocolo, método de coleta de sêmen, método de avaliação de SC e volume de sêmen, seleção da população, critérios de exclusão do estudo e número de amostras por homem). Foram registrados os intervalos de valores permitidos, tanto para variáveis categóricas quanto numéricas, e informações sobre a completude dos dados. Os dados foram extraídos da população total, bem como de todos os subgrupos elegíveis.
Controle de qualidade
O presente estudo seguiu o mesmo protocolo utilizado no estudo anterior. Para a nova busca, utilizamos o software de revisão sistemática Covidence para o processo de triagem dos artigos que não estavam disponíveis para nossa busca anterior. Além disso, um membro da equipe de pesquisa foi substituído. A triagem desta extensa revisão sistemática foi conduzida por uma equipe de oito revisores (HL, NJ, AM-A., JM, DW-D., MJ, RP, SHS). Como em nossa análise anterior, o protocolo de triagem foi testado e os revisores foram treinados pela triagem de 50 resumos por todos os revisores, seguida de uma comparação dos resultados, resolução de quaisquer inconsistências e esclarecimento do protocolo conforme necessário. O mesmo processo de controle de qualidade foi seguido para triagem do texto completo e extração de dados por todos os revisores. Todos os dados foram inseridos em planilhas digitais com valores permitidos explícitos (sem entradas abertas) para aumentar a consistência. Após a extração dos dados, uma rodada adicional de edição de dados e controle de qualidade de todos os estudos foi conduzida por HL e MJ. O processo garantiu que cada estudo fosse avaliado por pelo menos dois revisores treinados diferentes.
Análise estatística
Executamos todos os modelos tanto nos dados utilizados no nosso estudo de 2017 (para controle de qualidade) quanto no conjunto de dados incluindo todos os anos. Em todos os modelos, o ponto médio do período de coleta da amostra foi a variável independente (‘ano de coleta’) e a SC média (ou TSC) foi a(s) variável(ões) dependente(s). As unidades foram milhões/ml para SC e milhões para TSC (relatado ou definido como SC × volume de amostra). Todas as inclinações denotam mudança de unidade por ano civil, relatada com intervalos de confiança (IC) de 95%. Também reportamos valores do primeiro e último ano, e a variação percentual/ano.
Primeiramente utilizamos modelos de regressão linear simples para estimar SC e TSC em função do ano de coleta, com cada estudo ponderado pelo tamanho da amostra. Além de um modelo para todos os homens (Não Selecionados mais Férteis), também executamos um modelo estratificado por status de fertilidade.
Em seguida, usamos meta-regressão de efeitos aleatórios para modelar SC e TSC como funções lineares do tempo, ponderando as estimativas pelo erro padrão (SE).
Nos modelos de meta-regressão, controlamos um conjunto predeterminado de potenciais fatores de confusão: grupo de fertilidade, idade, tempo de abstinência, se os métodos de coleta e contagem de sêmen foram relatados, número de amostras por homem e indicadores para critérios de exclusão (Tabela Suplementar SII). O método utilizado para determinar o volume da amostra foi incluído na modelagem do TSC. Em todas as análises de metarregressão, incluímos variáveis indicadoras para denotar estudos com mais de uma estimativa de SC/TSC.
Várias variáveis foram imputadas, incluindo média de SC (e TSC), conforme descrito em nosso estudo de 2017. Por exemplo, para estudos que relataram mediana (não média) de SC ou TSC, estimamos a média adicionando a diferença média entre a média e a mediana em estudos para os quais ambas foram relatadas.
Incluímos indicadores em todos os modelos para valores imputados. Incluímos grupo continental (NEA ou SAA) e grupo de fertilidade (Não Selecionado ou Fértil), como variáveis no modelo quando aplicável.
Executamos vários modelos de meta-regressão para SC e TSC: (i) modelo básico não ajustado; (ii) modelo ajustado para todos os homens; (iii) estratificado por fecundidade; (iv) homens não selecionados apenas com interação tempo × continente; (v) todos os homens com duas interações: tempo × fertilidade e tempo × continente.
Estas análises foram repetidas para subconjuntos de coleta de dados para examinar tendências recentes (>1972, >1985, >1995 e >2000).
Realizamos diversas análises de sensibilidade: (i) adição de termos cúbicos e quadráticos para ano de coleta em análises de metarregressão para avaliar a não linearidade; (ii) remoção das covariáveis, uma de cada vez, do modelo; (iii) exclusão de um grupo específico, ou seja, o grupo sem informação sobre idade, para cada covariável; (iv) substituição da faixa etária pela média de idade, excluindo estudos que não reportaram média de idade; (v) adição de uma covariável para alta prevalência de tabagismo (>30%); (iv) remover cada continente, um de cada vez; (vii) exclusão de estudos com cinco ou mais pontos de dados para examinar a influência de grandes estudos; e (viii) remoção de estudos com SEs >20 milhões/ml.
Todas as análises foram realizadas no STATA versão 14.1 (StataCorp).
Resultados
Revisão sistemática e estatísticas resumidas
Usando pesquisas PubMed/MEDLINE e EMBASE, identificamos 2.936 novas publicações que atendem aos nossos critérios para triagem de resumos (Fig. 1). Destes, 151 registros duplicados foram removidos e 1.917 foram excluídos com base na triagem do título ou do resumo. Os textos completos dos 868 artigos restantes foram revisados para elegibilidade e 743 estudos foram excluídos. Dos 125 artigos restantes, 87 foram excluídos durante a extração de dados através da segunda rodada de triagem de texto completo; 44 deles eram publicações múltiplas. Os 38 estudos restantes de amostras de sêmen de 14.233 homens incluíram 44 estimativas médias únicas de SC que atendiam aos critérios do protocolo. Combinando estes novos dados com os dados da nossa metanálise anterior, a atual inclui resultados de 223 estudos, produzindo 288 estimativas baseadas em amostras de sémen coletas entre 1973 e 2018, fornecidas por 57.168 homens. Os dados estavam disponíveis em 6 continentes e 53 países (lista completa em Tabela Suplementar SIII e Figura complementar S1). Das 288 estimativas, 118 (41%) eram NEA não selecionadas, 35 (12%) eram SAA não selecionadas, 81 (28%) eram NEA férteis e 54 (19%) eram SAA férteis. O número de estimativas da SAA aumentou 29%.
Figura 1.
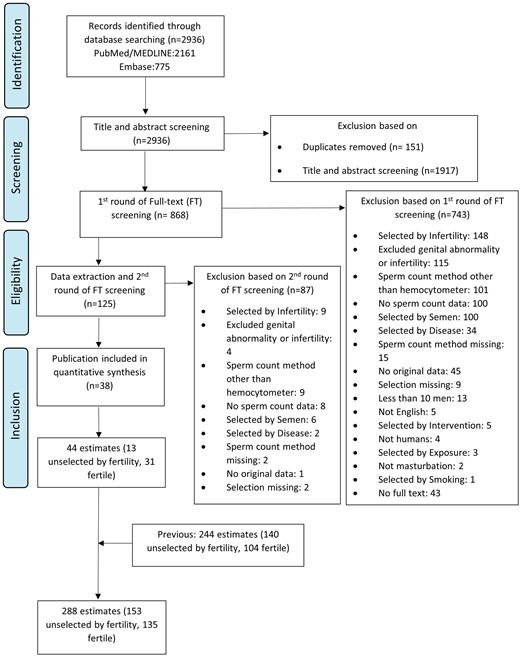
Fluxograma PRISMA mostrando a seleção dos estudos elegíveis para análise de metarregressão
Abrir em nova aba Baixar slide
Os dados das 223 publicações incluídas na metanálise estão disponíveis mediante solicitação razoável através do contato com o autor correspondente ( Abyholm, 1981 ; Fariss et al. , 1981 ; Leto e Frensilli, 1981 ; Wyrobek et al., 1981a, b; Aitken et al., 1981a, b ; Aitken et al. , 1981a , b ; al. , 1982 ; Nieschlag et al. , 1982 ; Obwaka et al. , 1982 ; Albertsen et al. , 1983 ; Fowler e Mariano, 1983 ; Sultan Sheriff, 1983 ; Wickingse outros. , 1983 ; Asch et al. , 1984 ; de Castro e Mastrorocco, 1984 ; Fredricsson e Sennerstam, 1984 ; Freischem et al. , 1984 ; Ward et ai. , 1984 ; Ayers et al. , 1985 ; Heussner et al. , 1985 ; Rosenberg et ai. , 1985 ; Aribarg et al. , 1986 ; Comhaire et al. , 1987 ; Kirei, 1987 ; Giblin et al. , 1988; Kjaergaard et al. , 1988 ; Mieusset et al. , 1988 , 1995 ; Jockenhovel et al. , 1989 ; Sobowale e Akiwumi, 1989 ; Svanborg et al. , 1989 ; Zhong e outros. , 1990 ; Culasso et al. , 1991 ; Dunphy et al. , 1991 ; Gottlieb et ai. , 1991 ; Nnatu et al. , 1991 ; Pangkahila, 1991 ; Weidner et al., 1991 ; Levine e outros. , 1992 ; Xerife e Legnain, 1992 ; Ali et ai. , 1993 ; Arce et al. , 1993 ; Bartoov et al. , 1993 ; Fedder et al. , 1993 ; Noack-Füller et al. , 1993 ; Organização Mundial da Saúde e Grupo de Trabalho sobre Métodos para a Regulação da Fertilidade Masculina, 1993 ; Hill et al. , 1994 ; Rehan, 1994 ; Rendon et al. , 1994 ; Tanejae outros. , 1994 ; Vanhoorne et al. , 1994 ; Auger et al. , 1995 ; Cottell e Harrison, 1995 ; Figà-Talamanca et al. , 1996 ; Fisch et al. , 1996 ; IrVine et al. , 1996 ; Van Waeleghem et al. , 1996 ; Vierula et al. , 1996 ; Vine et al. , 1996 ; Auger e Jouannet, 1997 ; Jensen et al. , 1997 ; Lemckee outros. , 1997 ; Handelsman, 1997a , b ; Chia et al. , 1998 ; Müller et al. , 1998 ; Naz et al. , 1998 ; Gyllenborg et al. , 1999 ; Kolstad et al. , 1999 ; Kuroki et al. , 1999 ; Larsen et al. , 1999 ; Purakayastha et al. , 1999 ; Reddy e Bordekar, 1999 ; De Celis et al. , 2000 ;Glazier et al. , 2000 ; Mak et al. , 2000 ; Selevan et al. , 2000 ; Wiltshire et al. , 2000 ; Zhang et ai. , 2000 ; Foppiani et al. , 2001 ; Guzick et al. , 2001 ; Hammadeh et ai. , 2001 ; Jørgensen et al. , 2001 , 2002 , 2011 , 2012 ; Kelleher et al. , 2001 ;Lee e Coughlin, 2001 ; Patankar et al. , 2001 ; També et al. , 2001 ; Xiao et ai. , 2001 ; Costello et al. , 2002 ; Junqing et al. , 2002 ; Kukuvitis et al. , 2002 ; Luetjens et al. , 2002 ; Punab et al. , 2002 ; Richthoff et al. , 2002 ; Danadevi et al. , 2003 ; de Gouveia Brazão et al. , 2003; Firman et al. , 2003 ; Liu et ai. , 2003 ; Lundwall et al. , 2003 ; Roste et al. , 2003 ; Serra-Majem et al. , 2003 ; Uhler et al. , 2003 ; Xu et al. , 2003 ; Ebesunun et al. , 2004 ; Rintala et al. , 2004 ; Toft et al. , 2004 , 2005 ; Bang et al. , 2005 ;Mahmoud et al. , 2005 ; Muthusami e Chinnaswamy, 2005 ; O’Donovan, 2005 ; Tsarev et al. , 2005 , 2009 ; Durazzo et al. , 2006 ; Fetic et al. , 2006 ; Giagulli e Carbone, 2006 ; Haugen et al. , 2006 ; Iwamoto et al. , 2006 , 2013a,b ; Pal et al. , 2006 ; Yucra et al. , 2006 ; Aneck-Hahn et al., 2007 ; Garcia e cols. , 2007 ; Multigner et al. , 2007 ; Plastira et al. , 2007 ; Rignell-Hydbom et al. , 2007 ; Wu e outros. , 2007 ; Akutsu et al. , 2008 ; Bhattacharya, 2008 ; Gallegos et al. , 2008 ; Goulis et al. , 2008 ; Jedrzejczak et al. , 2008 ; Kobayashi et ai. , 2008 ; Korovitse outros. , 2008 ; Li e Gu, 2008 ; López-Tijon et al. , 2008 ; Paasch et al. , 2008 ; Peters e outros. , 2008 ; Recabarren et al. , 2008 ; Recio-Vega et al. , 2008 ; Saxena et ai. , 2008 ; Shine et al. , 2008 ; Andrade-Rocha, 2009 ; Kumar et al. , 2009 , 2011 ; Rylander et al. , 2009 ;Stewart e outros. , 2009 ; Vani et al. , 2009 , 2012 ; Verit et al. , 2009 ; Engelbertz et al. , 2010 ; Hossain et al. , 2010 ; Ortiz et ai. , 2010 ; Rubes et al. , 2010 ; Tirumala Vani et al. , 2010 ; Al Momani et al. , 2011 ; Auger e Eustache, 2011 ; Axelsson et al. , 2011 ; Braheme outros. , 2011 ; Jacobsen et al. , 2011 ; Khan et al. , 2011 ; Linschooten et al. , 2011 ; Venkatesh et ai. , 2011 ; Vested et al. , 2011 ; Absalan et al. , 2012; Al-Janabi et al., 2012 ; Katukam et al. , 2012 ; Mostafa et al. , 2012 ; Nikoobakht et al. , 2012 ; Rabelo-Júnior et al. , 2012 ; Splingarte outros. , 2012 ; Bujan et al. , 2013 ; Girela et al. , 2013 ; Halling et al. , 2013 ; Ji et al. , 2013 ; Mendiola et al. , 2013 ; Redmon et al. , 2013 ; Thilagavathi et al. , 2013 ; Valsa et al. , 2013 ; Zalata et al. , 2013 ; Zareba et al. , 2013 ; Huang e outros. , 2014 ;Castiglione et ai. , 2014 ; Giagulli et al. , 2014 ; Kavitha e Malini, 2014 ; Liu et ai. , 2014 ; Mendiola et al. , 2014 ; Tainio et al. , 2014 ; Evgeni et al. , 2015 ; Franken, 2015 ; Hosen et al. , 2015 ; Layali et al. , 2015 ; Maomé et al. , 2015 ; Ramzan et al. , 2015 ; Romero-Oteroe outros. , 2015 ; Tsao et al. , 2015 ; Valsa et al. , 2015 ; Altintas et al. , 2016 ; Karimian e Colagar, 2016 ; Malić Vončina et al. , 2016 ; Shirota et al. , 2016 ; Malini, 2017 ; Mínguez-Alarcón et al. , 2017 ; Pullar et al. , 2017 ; Azad et ai. , 2018 ; Fanny et al. , 2018 ; Inih et al., 2018 ; López-Espín et al. , 2018 ; Lotti et al. , 2018 ; Palani, 2018 ; Priskorn et al. , 2018 ; Recio-Vega et al. , 2018 ; Ahmed et al. , 2019 ; Bassey et al ., 2019 ; Dhawan et al. , 2019 ; García Rodríguez et al. , 2019 ; Lazzarino et al. , 2019 ; Rodprasert et al. , 2019 ; Antônioe outros. , 2020 ; Dias e cols. , 2020 ).
Modelos lineares simples
Combinando os resultados de todos os homens, a SC diminuiu acentuadamente (inclinação por ano –0,87 milhões/ml; IC 95%: –0,89 a –0,86; P < 0,001) entre 1973 e 2018 ao usar modelos lineares simples, não ajustados e ponderados pelo tamanho da amostra (Tabela Suplementar SIV ,Suplementar Fig. S2). Para todos os homens combinados, o SC diminuiu 0,93% ao ano e, no geral, 41,5% entre 1973 e 2018. Num modelo estratificado por grupo de fertilidade, a inclinação foi muito mais acentuada para os Não Selecionados (–1,23; –1,25 a –1,20; P < 0,001) do que para homens férteis (–0,30; –0,33 a –0,27; P < 0,001) (Tabela Suplementar SIV). Uma tendência semelhante foi observada para TSC ao combinar os dois grupos de fertilidade (inclinação por ano = –2,80 milhões; –2,86 a –2,74; P <0,001), e a inclinação foi mais acentuada para o grupo Não Selecionado (–3,77; –3,83 a – 3,71; P < 0,001) (Tabela Suplementar SIV ,Suplementar Fig. S2). O volume de sêmen não se alterou durante o período do estudo (inclinação por ano = 0,0002 ml; –0,0001 a 0,0005; P = 0,249).
Modelos de meta-regressão para SC
Num modelo básico de meta-regressão para SC, no qual as estimativas foram ponderadas pelo seu SE, mas sem ajuste de covariáveis, as inclinações foram ligeiramente menos acentuadas do que para o modelo de regressão simples, e com ICs mais amplos (inclinação por ano –0,66 milhões/ml; 95 IC %: –0,92 a –0,40; P < 0,001). O ajuste de covariáveis não alterou sensivelmente a inclinação, mas ampliou ainda mais o IC (–0,59; –0,90 a –0,27; P < 0,001) (Tabela I , betas para covariáveis em Tabela Suplementar SII).
Concentração espermática (SC/sperm concentration) e contagem total de espermatozoides (TSC/total sperm count) no primeiro e último ano da análise de meta-regressão, ajustada para continentes e potenciais confundidores, a com variação percentual inclinação por ano: (i) total; (ii) estratificado por fecundidade; (iii) homens não selecionados apenas com interação tempo × continente; (iv) duas interações: tempo × fertilidade e tempo × continente.
| Modelo | Categoria | N (estimativas) | Primeiro ano | Primeiro ano SC (milhões/ml) | Ano passado | Ano passado SC (milhões/ml) | % alteração/ano | Inclinação (IC 95%), milhões/ml/ano |
|---|---|---|---|---|---|---|---|---|
| Total | Todos os homens | 288 | 1973 | 83,5 | 2018 | 57.1 | –0,71 | –0,59 (–0,90 a –0,27) |
| Estratificado | Não selecionado | 153 | 1973 | 101.2 | 2018 | 49,0 | –1,16 | –1,17 (–1,66 a –0,68) |
| Fertil | 135 | 1977 | 77.3 | 2017 | 72,8 | –0,14 | –0,11 (–0,54 a 0,32) | |
| Desmarcado com interação | NEA b não selecionado | 118 | 1973 | 103,7 | 2015 | 49,1 | –1,25 | –1,30 (–1,89 a –0,71) |
| SAA b não selecionado | 35 | 1986 | 88,3 | 2018 | 61,2 | –0,96 | –0,84 (–1,82 a 0,13) | |
| Duas interações | NEA b não selecionado | 118 | 1973 | 100,3 | 2015 | 46,8 | –1,27 | –1,27 (–1,78 a –0,77) |
| SAA b não selecionado | 35 | 1986 | 75,8 | 2018 | 54,9 | –0,86 | –0,65 (–1,29 a –0,01) | |
| NEA fértil | 81 | 1977 | 85,5 | 2017 | 65.1 | –0,59 | –0,50 (–1,00 a –0,01) | |
| SAA fértil | 54 | 1978 | 71,5 | 2016 | 76,4 | 0,18 | 0,13 (–0,42 a 0,67) |
| Modelo | Categoria | N (estimativas) | Primeiro ano | TSC do primeiro ano (milhões) | Ano passado | TSC do ano passado (milhões) | % alteração/ano | Inclinação (IC 95%), milhões/ano |
|---|---|---|---|---|---|---|---|---|
| Total | Todos os homens | 288 | 1973 | 297,4 | 2018 | 205.6 | –0,69 | –2,06 (–3,25 a –0,87) |
| Estratificado | Não selecionado | 153 | 1973 | 335,7 | 2018 | 126,6 | –1,40 | –4,70 (–6,56 a –2,83) |
| Fertil | 135 | 1977 | 305,8 | 2017 | 296.1 | –0,08 | –0,24 (–1,99 a 1,52) | |
| Desmarcado com interação | NEA b não selecionado | 118 | 1973 | 337,9 | 2015 | 125,9 | –1,49 | –5,05 (–7,31 a –2,79) |
| SAA b não selecionado | 35 | 1986 | 263.2 | 2018 | 141,7 | –1,44 | –3,79 (–7,58 a –0,01) | |
| Duas interações | NEA b não selecionado | 118 | 1973 | 350,9 | 2015 | 153,3 | –1,34 | –4,71 (–6,53 a –2,88) |
| SAA b não selecionado | 35 | 1986 | 229,8 | 2018 | 173,0 | –0,77 | –1,78 (–4,10 a 0,55) | |
| NEA fértil | 81 | 1977 | 303,8 | 2017 | 219.3 | –0,69 | –2,09 (–3,86 a –0,32) | |
| SAA fértil | 54 | 1978 | 216,6 | 2016 | 250,2 | 0,40 | 0,87 (–1,11 a 2,85) |
a . Modelo de meta-regressão, ajustado para continentes, idade, tempo de abstinência, método de coleta de sêmen relatado, método de contagem relatado, ter mais de uma amostra por homem, indicadores para seleção da população do estudo e critérios de exclusão (alguns candidatos à vasectomia, alguns candidatos a doadores de sêmen, exclusão de homens com doenças crônicas, exclusão por outros motivos não relacionados à fertilidade, seleção por ocupação não relacionada à fertilidade), se o ano de coleta foi estimado, se a média aritmética de SC foi estimada, se o SE de SC foi estimado e a variável indicadora a ser denotada estudos com mais de uma estimativa. Modelos de meta-regressão da concentração espermática (SC) ponderados por SC SE, ajustados para covariáveis semelhantes e método utilizado para avaliar o volume de sêmen. Modelos de meta-regressão de contagem total de espermatozoides (TSC) ponderados por TSC SE, ajustado para covariáveis semelhantes e método utilizado para avaliar o volume de sêmen.
b . NEA, América do Norte–Europa–Austrália; SAA, América do Sul/Central–Ásia–África.
Após estratificação por grupo de fertilidade e ajuste para todas as covariáveis, incluindo o grupo continental, houve um forte declínio na SC entre homens não selecionados (–1,17; –1,66 a –0,68; P < 0,001), mas não entre homens férteis (–0,11; –0,54 a 0,32; P = 0,615) (Tabela I , Fig. 2). Utilizando estimativas do modelo de SC de 101,2 milhões/ml em 1973 e 49,0 milhões/ml em 2018, a SC diminuiu entre os homens não seleccionados em 1,16% ao ano e 51,6% no geral (Tabela I ) .
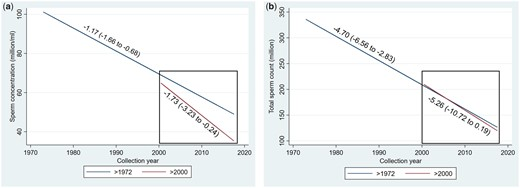
Figura 2.
Abrir em nova aba Baixar slide
Modelos de meta-regressão para concentração média de espermatozoides (SC) e contagem total de espermatozoides (TSC) por ano de coleta entre homens não selecionados de todos os continentes, ajustados para potenciais fatores de confusão, para todo o período e restritos a estudos posteriores a 2000. (a) Concentração espermática. ( b) Contagem total de espermatozoides. Modelo de meta-regressão ponderado pela concentração espermática (SC) SE, ajustado para continentes, idade, tempo de abstinência, método de coleta de sêmen relatado, método de contagem relatado, ter mais de uma amostra por homem, indicadores para seleção da população do estudo e critérios de exclusão (alguns candidatos a vasectomia, alguns candidatos a doadores de sêmen, exclusão de homens com doenças crônicas, exclusão por outros motivos não relacionados à fertilidade, seleção por ocupação não relacionada à fertilidade), se foi estimado o ano de coleta, se foi estimada a média aritmética de SC, se o SE de A SC foi estimada e variável indicadora para denotar estudos com mais de uma estimativa. Modelos de meta-regressão de contagem total de espermatozoides (TSC) ponderados por TSC SE, ajustados para covariáveis semelhantes e método utilizado para avaliar o volume de sêmen. SE, erro padrão.
Em um modelo de meta-regressão ajustado entre homens não selecionados que incluiu interação por grupo geográfico (P para interação = 0,44), a inclinação para NEA não selecionada foi –1,30 (–1,89 a –0,71; P <0,001) e a inclinação para SAA não selecionada foi –0,84 (–1,82 a 0,13, P = 0,088) ( Tabela I , Fig. 3 ).
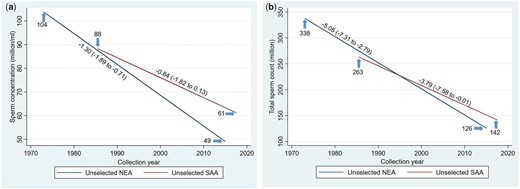
Abrir em nova aba Baixar slide
Modelos de meta-regressão para concentração média de espermatozoides (SC) e contagem total de espermatozoides (TSC) por ano de coleta com interação por continentes entre homens não selecionados, ajustados para potenciais fatores de confusão. ( a ) Concentração espermática (SC). ( b ) Contagem total de espermatozoides. NEA, América do Norte–Europa–Austrália; SAA, América do Sul/Central–Ásia–África. Modelo de meta-regressão ponderado pela concentração espermática (SC) SE, ajustado para continentes, idade, tempo de abstinência, método de coleta de sêmen relatado, método de contagem relatado, ter mais de uma amostra por homem, indicadores para seleção da população do estudo e critérios de exclusão (alguns candidatos a vasectomia, alguns candidatos a doadores de sêmen, exclusão de homens com doenças crônicas, exclusão por outros motivos não relacionados à fertilidade, seleção por ocupação não relacionada à fertilidade), se foi estimado o ano de coleta, se foi estimada a média aritmética de SC, se o SE de A SC foi estimada e variável indicadora para denotar estudos com mais de uma estimativa. Modelos de meta-regressão de contagem total de espermatozóides (TSC) ponderados por TSC SE, ajustado para covariáveis semelhantes e método utilizado para avaliar o volume de sêmen. SE, erro padrão.
Em um modelo de meta-regressão ajustado, que incluiu todos os homens e dois termos de interação [tempo × grupo de fertilidade (P = 0,012) e tempo × continentes ( P = 0,058)], foram observados declínios entre NEA não selecionados (–1,27; –1,78 para –0,77; P < 0,001), SAA Não Selecionado (–0,65; –1,29 a –0,01; P = 0,045) e NEA Fértil (–0,50; –1,00 a –0,01; P = 0,046) (Tabela I ,Figura complementar S3).
Modelos de meta-regressão para TSC
No geral, as tendências da TSC foram semelhantes às da SC. Num modelo de meta-regressão ajustado para todos os homens, houve um declínio acentuado na TSC (inclinação por ano –2,06 milhões, –3,25 a –0,87; P = 0,001) (Tabela I).
Após estratificação por grupo de fertilidade e ajuste para todas as covariáveis, incluindo continente, houve um forte declínio na TSC entre homens não selecionados (–4,70; –6,56 a –2,83; P <0,001), mas não entre homens férteis (–0,24; –1,99 a 1,52). ; P = 0,788) ( Tabela I , Figura 2 ). Utilizando estimativas do modelo TSC de 335,7 milhões em 1973 e 126,6 milhões em 2018, a TSC diminuiu entre os homens não seleccionados em 1,40% ao ano e 62,3% no geral ( Tabela I ).
Em um modelo de meta-regressão ajustado entre homens não selecionados, incluindo interação por grupo geográfico ( P para interação = 0,44), a inclinação para NEA não selecionada foi de –5,05 (–7,31 a –2,79; P <0,001) e a inclinação para SAA não selecionada foi –3,79 (–7,58 a –0,01, P = 0,049) (Tabela I , Fig. 3).
Em um modelo de meta-regressão ajustado, que incluiu todos os homens e dois termos de interação [tempo × grupo de fertilidade ( P = 0,013) e tempo × continentes (P = 0,015)], foram observados declínios entre NEA não selecionados (–4,71; –6,53 para –2,88; P < 0,001), SAA Não Selecionado (–1,78; –4,10 a 0,55; P = 0,133) e NEA Fértil (–2,09; –3,86 a –0,32; P = 0,021) ( Tabela I ,Figura complementar S3 ).
Modelos de meta-regressão para períodos recentes
Também restringimos a análise de homens não selecionados (em todos os continentes) a intervalos de tempo recentes (Tabela II , Fig. 2). Após 1995, a inclinação para SC foi um pouco mais acentuada (–1,33; –2,41 a –0,26; P = 0,016) e foi ainda mais acentuada após 2000 (–1,73; –3,23 a –0,24; P = 0,024). Houve um aumento acentuado no declínio percentual em SC por ano no período recente, de 1,16% pós-1972 para 2,64% pós-2000 (Fig. 4). Pós-2000, a inclinação do TSC (–5,26, –10,72 a 0,19; P = 0,058) também foi mais acentuada do que a do pós-1972 (Tabela II , Fig. 2).
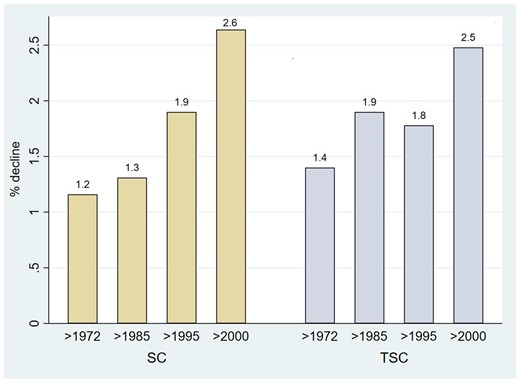
Abrir em nova aba Baixar slide
Porcentagem de declínio de acordo com os períodos, para concentração média de espermatozoides (SC) e contagem total de espermatozoides (TSC) entre homens não selecionados usando modelo de meta-regressão estratificada. Modelo de meta-regressão estratificada ponderada pela concentração espermática (SC) SE, ajustado para continentes, idade, tempo de abstinência, método de coleta de sêmen relatado, método de contagem relatado, ter mais de uma amostra por homem, indicadores para seleção da população do estudo e critérios de exclusão (alguns candidatos à vasectomia, alguns candidatos a doadores de sêmen, exclusão de homens com doenças crônicas, exclusão por outros motivos não relacionados à fertilidade, seleção por ocupação não relacionada à fertilidade), se foi estimado o ano de coleta, se foi estimada a média aritmética de SC, se SE foi estimado de SC foi estimada e variável indicadora para denotar estudos com mais de uma estimativa. Modelos de meta-regressão estratificada de contagem total de espermatozoides (TSC) ponderados por TSC SE, ajustados para covariáveis semelhantes e método utilizado para avaliar o volume de sêmen. SE, erro padrão.
Modelo de meta-regressão estratificada a para concentração média de espermatozoides (SC) e contagem média total de espermatozoides (TSC) entre homens não selecionados, por períodos.
| Período (anos) | N (estimativas) | Primeiro ano | Primeiro ano SC (milhões/ml) | Ano passado | Ano passado SC (milhões/ml) | % de variação/ano | Inclinação (IC 95%), milhões/ml/ano |
|---|---|---|---|---|---|---|---|
| >1972 | 153 | 1973 | 101.2 | 2018 | 49,0 | –1,16 | –1,17 (–1,66 a –0,68) |
| >1985 | 131 | 1985 | 82.3 | 2018 | 47.1 | –1,31 | –1,08 (–1,68 a –0,49) |
| >1995 | 89 | 1995 | 70.1 | 2018 | 40.1 | –1,90 | –1,33 (–2,41 a –0,26) |
| >2000 | 60 | 2000 | 65,6 | 2018 | 35,3 | –2,64 | –1,73 (–3,23 a –0,24) |
| Período (anos) | N (estimativas) | Primeiro ano | TSC do primeiro ano (milhões) | Ano passado | TSC do ano passado (milhões) | % de variação/ano | Inclinação (IC 95%), milhões/ano |
|---|---|---|---|---|---|---|---|
| >1972 | 153 | 1973 | 335,7 | 2018 | 126,6 | –1,40 | –4,70 (–6,56 a –2,83) |
| >1985 | 131 | 1985 | 275.2 | 2018 | 105,6 | –1,90 | –5,22 (–7,62 a –2,82) |
| >1995 | 89 | 1995 | 231.1 | 2018 | 138,5 | –1,78 | –4,11 (–8,21 a –0,02) |
| >2000 | 60 | 2000 | 212.1 | 2018 | 120,0 | –2,48 | –5,26 (–10,72 a 0,19) |
a . Modelo de meta-regressão estratificada, ajustado para continentes, idade, tempo de abstinência, método de coleta de sêmen relatado, método de contagem relatado, ter mais de uma amostra por homem, indicadores para seleção da população do estudo e critérios de exclusão (alguns candidatos à vasectomia, alguns candidatos a doadores de sêmen , exclusão de homens com doenças crônicas, exclusão por outros motivos não relacionados à fecundidade, seleção por ocupação não relacionada à fecundidade), se foi estimado o ano de coleta, se foi estimada a média aritmética de SC, se foi estimado o SE de SC e a variável indicadora para denotam estudos com mais de uma estimativa. Modelos de metarregressão da concentração espermática (SC) ponderados por SC SE, ajustados para covariáveis semelhantes e método utilizado para avaliar o volume de sêmen. Modelos de meta-regressão de contagem total de espermatozóides (TSC) ponderados por TSC SE, ajustado para covariáveis semelhantes e método utilizado para avaliar o volume de sêmen.
Análises de sensibilidade
Realizamos múltiplas análises para examinar a sensibilidade dos resultados às suposições sobre nosso modelo, linearidade, influência de covariáveis e imputação de dados faltantes. Os resultados das análises de sensibilidade são mostrados aqui apenas para SC em homens não selecionados (inclinação = –1,17 milhões/ml/ano no modelo principal). Em todas as análises de sensibilidade (exceto uma elaborada a seguir), houve um forte declínio (>1,0 milhão/ml/ano) na SC no grupo Não Selecionado, com P < 0,01.
Adicionar uma função quadrática ou cúbica de ano ao modelo de meta-regressão não alterou substancialmente a associação entre ano e SC nem melhorou o ajuste do modelo: coeficiente para o termo quadrático: 0,04; IC 95%: –0,07 a 0,08, P = 0,135; para o termo cúbico 0,0005; IC 95%: –0,0007 a 0,001, P = 0,086).
Para cada covariável, realizamos duas análises de sensibilidade: (i) removendo a covariável e (ii) excluindo um grupo específico, para cada covariável (Tabela Suplementar SV). Excluindo 47 estimativas sem dados sobre a idade média e ajustando para a idade média em vez da faixa etária, obteve-se uma inclinação de –1,27 milhões/ml/ano (–1,86 a –0,68; P < 0,001), que é semelhante ao modelo principal. A análise de sensibilidade que mostrou uma alteração mais do que mínima no declive foi a exclusão de 39 estimativas sem informação sobre a idade, o que resultou num declive ligeiramente diminuído de –0,94 milhões/ml/ano (–1,51 a –0,37, P = 0,002).
A proporção de fumantes foi relatada em apenas 26,0% dos estudos e em 18,1% dos estudos de homens não selecionados. Para examinar esta variável, realizamos uma análise de sensibilidade incluindo uma covariável para “alta proporção de fumantes” (> 30%), e as inclinações mudaram apenas ligeiramente (–1,20 milhões/ml, –1,70 a –0,71; P < 0,001).
Os resultados para homens não selecionados não mudaram materialmente com análises de sensibilidade adicionais, pela exclusão de estimativas de qualquer continente específico (Tabela Suplementar SVI ). As inclinações também foram robustas após a exclusão dos quatro estudos com cinco ou mais pontos de dados (-1,04, -1,55 a -0,53; P <0,001), ou exclusão de cinco estimativas com um SE de SC > 20 milhões/ml (-1,11, -1,61 a –0,62; P < 0,001).
Devido a um erro de digitação no valor extraído para Rubes et al. (2010) na metanálise anterior, repetimos a análise sem este estudo e também com o valor corrigido. Os resultados não mudaram materialmente.
Discussão
Os resultados do presente estudo ampliam os da nossa metanálise de 2017. Conforme detalhado abaixo, os novos dados permitem novas análises e novos resultados. Fornecemos fortes evidências, pela primeira vez, de um declínio na contagem de espermatozoides entre homens da América do Sul/Central, Ásia e África, bem como de um declínio mundial no século XXI, com dados que sugerem que o ritmo deste o declínio acelerou.
Principais conclusões
Em nossa revisão sistemática e metanálise anteriores (Levine et al. , 2017), relatamos um declínio acentuado e contínuo na SC e na TSC na América do Norte, Europa e Austrália com base em amostras coletadas entre 1973 e 2011. O que há de novo em a análise atual?
Nossa análise atual, a maior já realizada a examinar tendências temporais na contagem de espermatozoides, amplia tanto o período de estudo quanto o número de estimativas. Esta nova análise inclui sete anos adicionais de coleta de amostras e acrescenta 44 estimativas às 244 incluídas na análise anterior. É, portanto, mais robusto e mais relevante temporalmente.
A distribuição dos países contribuintes mudou desde a nossa análise de 2017. A nova análise aumenta sensivelmente o número de estudos da SAA. Com este aumento no tamanho da amostra, existe agora poder adequado para examinar as tendências em SC e TSC nesses continentes. Esta análise fornece fortes evidências, pela primeira vez, de um declínio apreciável na contagem de espermatozoides entre homens não selecionados da SAA. É importante ressaltar que esta análise também demonstra um declínio acelerado na SC e na TSC pós-2000. Em resumo, esta atualização confirma, amplia e fortalece os resultados da nossa análise de 2017.
Comparação com estudos anteriores
A Tabela III compara as características básicas e os resultados do presente estudo com os de Carlsen et al . (1992) , Swan et al. (2000) e Levine et al. (2017) , estudos que juntos incluem dados coletados ao longo de mais de 80 anos. É notável que, embora os métodos de pesquisa e análise estatística tenham se tornado mais sofisticados e a distribuição dos estudos tenha mudado (com o aumento da proporção de SAA), essas inclinações são notavelmente consistentes.
Tabela III
Características e resultados do ajuste de um modelo de regressão linear simples (sem ajuste, ponderado pelo tamanho da amostra) para tendências de concentração de espermatozoides no presente estudo em comparação com estudos anteriores.
| Primeiro autor (ano de publicação) | Carlsen et al. (1992) | Cisne et al. (2000) | Levine e outros. ( 2017 ) | Levine e outros. (2022), artigo atual |
|---|---|---|---|---|
| anos de publicação | 1938–1990 | 1934–1996 | 1981–2013 | 1981–2019 |
| Número de estudos | 61 | 101 | 185 | 223 |
| Número de países | 20 | 28 | 50 | 53 |
| Grupo de fertilidade: N (%) | ||||
| Não selecionado | 22 (36%) | 50 (50%) | 140 (57%) | 153 (53%) |
| Fértil | 39 (64%) | 51 (50%) a | 104 (43%) | 135 (47%) |
| Continentes: N (%) | ||||
| NEA b | 45 (74%) | 78 (77%) | 175 (72%) | 199 (69%) |
| SAA | 16 (26%) | 23 (23%) | 69 (28%) | 89 (31%) |
| Declive | –0,93 | –0,94 | –0,70 | –0,87 |
| P -valor | <0,001 | <0,001 | <0,001 | <0,001 |
a . Esposa grávida ou no pós-parto ou pelo menos 90% dos homens com fertilidade comprovada.
b . NEA inclui estudos da América do Norte-Europa-Austrália. A SAA inclui estudos da América do Sul/Central–Ásia–África.
Comparando a análise atual com Levine et al. (2017, notamos que os métodos de busca e triagem da literatura, bem documentados em ambos, não mudaram, nem os métodos analíticos.
Tanto em nossas análises atuais quanto nas anteriores, excluímos estudos que selecionaram homens com base em critérios que provavelmente afetariam a contagem de espermatozoides (por exemplo, exigir uma contagem mínima de espermatozoides ou a participação dos homens em um banco de espermatozoides), com uma exceção. Estudos de homens férteis foram incluídos como um estrato separado (denotado Fértil). Este grupo de estudos inclui pais ou parceiros de gestantes. Assim, esses homens ajudaram eles próprios a conceber uma gravidez ou a gravidez foi resultado de fertilização in vitro (FIV). A proporção de nascimentos por fertilização in vitro aumentou durante o período de estudo desta análise, com oito milhões de bebês nascidos por fertilização in vitro em todo o mundo desde o primeiro nascimento por fertilização in vitro no mundo em 1978 (Sociedade Europeia de Reprodução Humana e Embriologia, 2018). Entre os 135 estudos categorizados como férteis nesta análise, apenas 27,4% excluíram explicitamente as gestações concebidas por fertilização in vitro.
Aqui, tal como na nossa análise de 2017, estratificámos os países em dois grupos, devido ao potencial de confusão de tendências por geografia. No passado, referíamo-nos a estes dois grupos de países como “Ocidentais” e “Outros”. Embora não fosse a nossa intenção, tornou-se evidente que estes termos tinham o potencial de serem mal interpretados e politizados. Portanto, referimo-nos agora a estes dois grupos de estudos por continente em que os dados foram recolhidos: ‘NEA‘ (América do Norte, Europa e Austrália) e ‘SAA‘ (América do Sul/Central, África e Ásia). Apresentamos resultados estratificados por grupo continental, bem como combinados.
Outros problemas
Poderiam os declínios que relatamos ser simplesmente o resultado de uma diminuição aleatória num padrão de flutuações (denominado ‘variabilidade espermática’) (Boulicault et al., 2021 )? O declínio contínuo demonstrado nesta e em meta-análises anteriores fornece fortes evidências de que este não é o caso. Se, de facto, os declínios que relatamos fossem meramente o resultado de flutuações aleatórias na contagem de espermatozoides, esperaríamos, em média, que uma percentagem de estudos não relatasse nenhuma alteração e o restante reportasse (aproximadamente) um número igual de aumentos e diminui. A literatura não apoia isso (Jørgensen et al., 2021 ; Aitken, 2022).
Embora a contagem de espermatozoides seja um proxy imperfeito para a fertilidade, a SC e a TSC estão intimamente ligados às chances de fertilidade (Guzick et al. , 2001). A relação entre SC e tempo até a concepção não é linear. Assim, após um limiar de 40-50 milhões/ml, um SC mais elevado não implica necessariamente uma maior probabilidade de concepção. Por outro lado, abaixo desse limite, a probabilidade de concepção diminui rapidamente à medida que a SC diminui (Bonde et al., 1998). A nível populacional, a queda na média da SC de 104 para 49 milhões/ml que aqui relatamos implica um aumento substancial na proporção de homens com atraso na concepção. Assim, a SC fornece a medida mais estável e confiável para comparações dentro e entre populações e ao longo do tempo.
Forças
Neste estudo, assim como em Levine et al. (2017, utilizamos protocolos escritos e extensos procedimentos de controle de qualidade que minimizaram potenciais vieses de informação e seleção em todas as etapas do estudo. Outros pontos fortes deste estudo incluem nossa pesquisa bibliográfica completa e documentada, a revisão de todos os artigos recuperados por dois membros da equipe do estudo e o uso de métodos meta-analíticos atuais. Todas as estimativas foram ponderadas pelo SE da medição e todas as premissas foram examinadas em análises de sensibilidade. Neste estudo, reexecutamos todas as etapas das meta-análises anteriores no conjunto maior de dados combinados, bem como nas publicações recém-recuperadas.
Nosso grande número de estudos e pontos de dados nos permitiu controlar um conjunto pré-determinado de covariáveis, bem como a modificação por status de fertilidade e grupo geográfico e variáveis que indicam a integridade dos dados e critérios de exclusão do estudo.
Os métodos que utilizamos para a revisão sistemática da literatura e metanálise são os mais atuais e amplamente aceitos pela comunidade científica.
Limitações
Analisamos a contagem de espermatozoides (SC e TSC), mas não a motilidade e morfologia dos espermatozoides. A interpretação das tendências na motilidade e morfologia dos espermatozoides é difícil, uma vez que os métodos mudaram acentuadamente durante o período de estudo. No entanto, os métodos para medir a SC permaneceram praticamente inalterados. A contagem por hemocitômetro é a forma clássica de avaliar a SC e tem sido recomendada pela Organização Mundial da Saúde em todas as versões dos manuais de análise de sêmen das organizações (Wang et al. , 2022).
Caso nenhum método de contagem fosse indicado ou fosse relatado o uso de outro método que não o hemocitômetro, o estudo era excluído. No geral, 334 estudos foram excluídos porque foi utilizado um método diferente do hemocitômetro, enquanto 128 estudos foram excluídos porque nenhum método de contagem de espermatozoides foi fornecido. Das 288 estimativas para SC e TSC incluídas, cerca de metade (146) foram provenientes de estudos que declararam explicitamente que um hemocitômetro foi utilizado. As 142 estimativas restantes foram provenientes de estudos que utilizaram métodos da Organização Mundial da Saúde, sem nomear o tipo específico de hemocitômetro utilizado. Incluímos ambos os grupos de estudos em nossas análises juntamente com uma variável indicando se o hemocitômetro havia sido nomeado explicitamente como método de contagem. Nas análises de sensibilidade,
A eliminação completa de todos os vieses de seleção/recrutamento é impossível, uma vez que não é possível coletar amostras de sêmen aleatoriamente. No entanto, minimizamos o viés de recrutamento avaliando os métodos de recrutamento em todos os estudos incluídos. Conforme declarado em Métodos, os estudos que selecionaram homens com base em qualquer variável conhecida por afetar a contagem de espermatozoides não foram elegíveis. Isto inclui estudos que selecionaram homens com base num parâmetro do sêmen, numa condição associada a um parâmetro do sêmen (como a varicocele) ou numa exposição ou ocupação associada à sua qualidade. Contudo, incluímos os homens “férteis” como um grupo separado, embora este seja um grupo selecionado. Em comparação com os homens não selecionados, a inclinação para os homens férteis foi mais modesta do que a dos homens não selecionados da NEA, e não foi observado qualquer declínio entre os homens férteis da SAA. Os homens classificados como “férteis” são problemáticos de diversas maneiras. Em primeiro lugar, incluem tanto aqueles cujo parceiro concebeu sem assistência médica como com assistência médica, cuja fração variou consoante o tempo e o local. Em segundo lugar, os homens com menor qualidade de sêmen estão sub-representados entre os homens férteis. Mudanças na proporção de homens férteis na população ao longo do tempo podem levar a um viés de seleção no grupo Fértil. Em contraste, o grupo Não Selecionado não está sujeito a esse viés de seleção.
Também é possível que os homens que fornecem uma amostra de sêmen sejam diferentes daqueles que não o fazem. Estudamos anteriormente esta importante questão comparando os níveis de testosterona e de inibina B em homens não selecionados (potenciais recrutas militares submetidos a um exame físico de rotina obrigatório para determinar a sua aptidão para o serviço militar) que concordaram em entregar uma amostra de sêmen aos homens que apenas concordaram em dar uma amostra de sangue. Em ambos os grupos de homens, os níveis hormonais foram semelhantes (Andersen et al. , 2000). Portanto, o viés de recrutamento é improvável em estudos com homens não selecionados.
Tal como na nossa análise anterior, incluímos apenas publicações em língua inglesa, o que foi inevitável dada a dimensão da tarefa e o tamanho limitado da nossa equipa de estudo. No entanto, das 2.936 publicações identificadas através de nossas pesquisas em bancos de dados em 2020, apenas 49 foram excluídas devido ao idioma.
Além disso, seria interessante explorar as tendências na contagem de espermatozoides num continente específico ou mesmo dentro de países e subpopulações. Contudo, não tínhamos poder estatístico adequado para examinar esta questão a um nível geográfico mais preciso. Estudos repetidos sobre a qualidade do sêmen em populações específicas complementariam o estudo atual, fornecendo informações sobre tendências locais.
Conclusão e implicações mais amplas
Os nossos novos dados e análises confirmam as nossas descobertas anteriores de um declínio apreciável na contagem de espermatozoides entre 1973 e 2018 entre homens da América do Norte, Europa e Austrália e apoiam um declínio entre homens não selecionados da América do Sul/Central, África e Ásia. Este declínio continuou, conforme previsto pela nossa análise anterior, e tornou-se mais acentuado desde 2000. Este declínio substancial e persistente é agora reconhecido como um problema significativo de saúde pública. Em 2018, um grupo de médicos e cientistas líderes apelou aos governos para que reconhecessem a diminuição da fertilidade masculina como um importante problema de saúde pública e para que reconhecessem a importância da saúde reprodutiva masculina para a sobrevivência da espécie humana (e de outras) (Levine et al., 2018). São necessárias pesquisas sobre as causas deste declínio contínuo e uma resposta imediata e focada para evitar maiores perturbações na saúde reprodutiva masculina.
Esperamos que as novas evidências aqui fornecidas recebam a atenção não só dos médicos e cientistas, mas também daqueles que tomam decisões públicas e da população em geral.
Dados suplementares
Dados suplementares estão disponíveis em Human Reproduction Update online.
Disponibilidade de dados
Os dados subjacentes a este artigo serão compartilhados mediante solicitação razoável ao autor correspondente.
Reconhecimentos
Agradecemos a Alexandria Albert por sua assistência na revisão da literatura.
Funções dos autores
A HL teve acesso total a todos os dados e assume a responsabilidade pela integridade dos dados e pela precisão da análise dos dados. Conceito e desenho do estudo: HL e SHS. Desenho e execução da estratégia de busca: HL e RP. Aquisição, análise ou interpretação dos dados: HL, NJ, AM-A., JM, DW-D., MJ, RP e SHS. Redação do manuscrito : HL, SHS e MJ. Revisão crítica do manuscrito quanto ao conteúdo intelectual importante: HL, NJ, AM-A, JM, DW-D., MJ, RP e SHS. Análise estatística: HL e MJ. Apoio administrativo, técnico ou material: HL , RP, SHS e MJ. Supervisão do estudo: HL e SHS.
Financiamento
Reconhecemos com gratidão o apoio financeiro da Fundação Grantham para a Proteção do Meio Ambiente. Nenhuma das fontes de financiamento desempenhou um papel na concepção e condução do estudo; coleta, gestão, análise e interpretação dos dados; preparação, revisão ou aprovação do manuscrito; ou decisão de submeter o manuscrito para publicação. Anderson Martino-Andrade é bolsista do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq, Brasil).
Conflito de interesses
Todos os autores declaram não ter nenhum conflito de interesse.
Referências
NOTA DO WEBSITE: Infelizmente não conseguimos transpor a bibliografia apresentada de uma maneira adequada, por isso sugerimos que os interessados acessem o texto original para conhecimento:
https://academic.oup.com/humupd/article/29/2/157/6824414
© The Author(s) 2022. Published by Oxford University Press on behalf of European Society of Human Reproduction and Embryology. All rights reserved. For permissions, please email: [email protected]
This article is published and distributed under the terms of the Oxford University Press, Standard Journals Publication Model (https://academic.oup.com/pages/standard-publication-reuse-rights)
Dados suplementares
dmac035_Supplementary_Data – arquivo docx Publicidade destinada a profissionais de saúde
Tradução livre, parcial, de Luiz Jacques Saldanha, agosto de 2023.


