Somos o que comemos.
Analysis by Dr. Joseph Mercola
December 31, 2020
Resumo da história
- Uma proporção significativa de seu sistema imunológico reside no trato gastrointestinal. Os pesquisadores de Harvard identificaram agora a população específica de bactérias intestinais que modulam as respostas imunes localizadas e sistêmicas para repelirem invasores virais;
- Bacteroides fragilis e outras bactérias da família Bacteroides iniciam uma cascata de sinalização que induz a liberação de interferon-beta, que protege contra a invasão viral, estimulando as células do sistema imunológico a atacarem o vírus, causando a autodestruição das células infectadas pelo vírus;
- A permeabilidade intestinal mediada pela zonulina desempenha um papel determinante na patogênese de muitas doenças inflamatórias crônicas. A zonulina é produzida em resposta a bactérias nocivas. Ele elimina as bactérias abrindo as junções estreitas
- Além do super crescimento de bactérias, o glúten é um poderoso gatilho da liberação de zonulina, pois sua via interpreta erroneamente o glúten como um componente potencialmente prejudicial de um microorganismo;
- As doenças inflamatórias crônicas associadas à desregulação da via da zonulina e intestino permeável incluem distúrbios auto imunes, distúrbios metabólicos, doenças intestinais, doenças neuro-inflamatórias e câncer do cérebro e do fígado.
Mais atenção do que nunca está sendo dada à sua saúde intestinal e compreensivelmente, considerando que uma proporção significativa do seu sistema imunológico reside no seu trato gastrointestinal. 1 Como tal, otimizar o seu microbioma intestinal é uma busca que vale a pena, que terá efeitos de longo alcance na sua saúde física e bem-estar emocional.
Evidências científicas crescentes também continuam a sugerir um grande componente dos centros de nutrição na alimentação de bactérias promotoras da saúde em seu intestino (e em outras partes do corpo). Ao fazer isso, você mantém os micróbios nocivos sob controle e reforça sua proteção contra doenças crônicas.
A doença começa em seu intestino
TDAH, autismo , dificuldades de aprendizagem, obesidade, diabetes 2 e doença de Parkinson são apenas algumas das condições que são influenciadas pelo microbioma intestinal. Uma revisão científica de 2020 3 vai mais longe ao dizer que todas as doenças inflamatórias começam no intestino. Parte da culpa é atribuída à higiene excessiva. Em outras palavras, somos “limpos demais” para nosso próprio bem.
Mas sua dieta também desempenha um papel crucial. O artigo aborda especificamente o papel da permeabilidade intestinal mediada por zonulina na patogênese de doenças inflamatórias crônicas (CIDs). Segundo o autor, Dr. Alessio Fasano, 4 gastroenterologista pediátrico, pesquisador e diretor do Center for Celiac Research and Treatment: 5
“Além da composição genética e da exposição a gatilhos ambientais, aumento inadequado da permeabilidade intestinal (que pode ser influenciado pela composição da microbiota intestinal), um sistema imunológico ‘hiper-beligerante’ responsável pelo equilíbrio da tolerância-resposta imunológica e da composição do microbioma intestinal e sua influência epigenética na expressão genômica do hospedeiro foram identificados como três elementos adicionais em causar CIDs.
Durante a última década, um número crescente de publicações enfocou a genética humana, o microbioma intestinal e a proteômica, sugerindo que a perda da função de barreira da mucosa, particularmente no trato gastrointestinal, pode afetar substancialmente o tráfico de antígenos, em última análise, influenciando a interação bidirecional próxima entre microbioma intestinal e nosso sistema imunológico.
Essa conversa cruzada é altamente influente na formação da função do sistema imunológico do intestino do hospedeiro e, em última análise, na mudança da predisposição genética para o resultado clínico. Esta observação levou a uma revisitação das possíveis causas de epidemias de CIDs, sugerindo um papel patogênico chave da permeabilidade intestinal.
Estudos pré-clínicos e clínicos demonstraram que a família das zonulinas, um grupo de proteínas que modula a permeabilidade intestinal, está envolvida em uma variedade de CIDs, incluindo doenças autoimunes, infecciosas, metabólicas e tumorais. Esses dados oferecem novos alvos terapêuticos para uma variedade de CIDs em que a via da zonulina está implicada em sua patogênese. ”
Bactérias, não genes, governam o destino de nossa saúde
Fasano ressalta que simplesmente não temos genes suficientes para explicar a miríade de doenças crônicas que podem nos acometer. Os genes também não podem explicar o momento do início da doença. Para resolver esses mistérios, devemos olhar para o microbioma, diz ele, pois “é a interação entre nós como indivíduos e o ambiente em que vivemos que dita nosso destino clínico”.
Além dos próprios micróbios, a condição da mucosa intestinal também desempenha um papel significativo. “Embora essa enorme interface da mucosa (200 m2) não seja aparentemente visível, ela desempenha um papel central por meio de suas interações dinâmicas com uma variedade de fatores provenientes do ambiente circundante, incluindo microrganismos, nutrientes, poluentes e outros materiais”, explica Fasano.
Embora as junções estreitas intracelulares fossem consideradas estáticas e impermeáveis, agora sabemos que não é o caso. Conforme explicado por Fasano, a zonulina é um modulador poderoso da permeabilidade intestinal. No entanto, embora a zonulina seja um biomarcador da permeabilidade intestinal e desempenhe um papel patogênico em muitas doenças inflamatórias crônicas, nem todos os CIDs são causados por intestino permeável.
Cadeia de eventos proposta que leva ao CID
O gráfico abaixo, incluído na revisão de Fasano, mas originado de um artigo anterior 6 intitulado “Zonulina, um regulador de funções de barreira epitelial e endotelial e seu envolvimento em doenças inflamatórias crônicas”, co-escrito por Fasano e Craig Sturgeon, detalha a “proposta cadeia de eventos que levam à doença inflamatória crônica”.
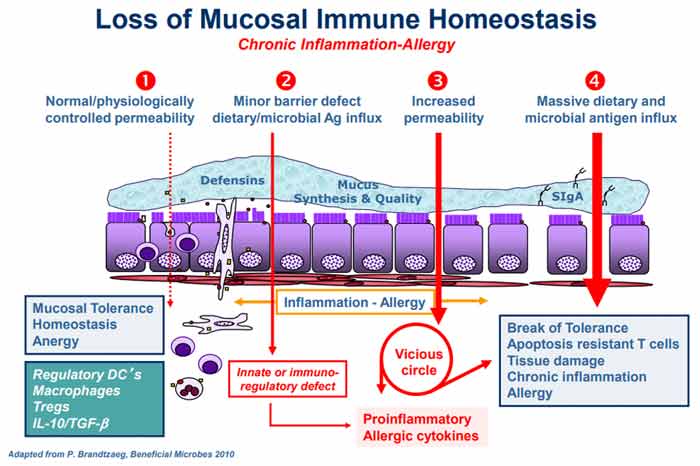
Em circunstâncias normais, uma homeostase saudável é mantida no revestimento do intestino de forma que quando um antígeno é encontrado, nenhuma reação imunológica excessiva ocorre (anergia). No nº 2 do gráfico, a disbiose intestinal está se instalando (ou seja, um desequilíbrio no número e na diversidade da microflora intestinal), causando um excesso de produção de zonulina, que por sua vez torna o revestimento intestinal mais permeável.
De acordo com Fasano, os dois gatilhos mais poderosos da liberação de zonulina são o crescimento excessivo de bactérias e o glúten. A zonulina é produzida em resposta a bactérias nocivas 7 – ajuda a expulsar as bactérias ao abrir as junções estreitas – portanto, o crescimento excessivo de bactérias faz sentido. Mas por que ele responde ao glúten?
Curiosamente, a via da zonulina interpreta erroneamente o glúten como um componente potencialmente prejudicial de um microorganismo. É por isso que o glúten desencadeia a liberação de zonulina. Embora não seja mencionado por Fasano, o herbicida glifosato também ativa a zonulina e é 10 vezes mais potente que o glúten! 8
A permeabilidade subsequente permite que o antígeno derivado da microbiota e a endotoxina migrem do lúmen para a lâmina própria (o tecido conjuntivo que faz parte da membrana mucosa que reveste o intestino), desencadeando assim a inflamação.
Conforme o processo continua a piorar (Nº 3 no gráfico), sua resposta imune adaptativa é ativada, desencadeando a produção de citocinas pró-inflamatórias, incluindo interferon gama (IFN-γ) e fator de necrose tumoral alfa (TNF-α). Essas citocinas pioram ainda mais a permeabilidade, criando um ciclo vicioso. Eventualmente (Nº 4), a tolerância da mucosa é completamente rompida, resultando no início de uma doença inflamatória crônica.
Doenças inflamatórias crônicas relacionadas ao intestino gotejante
A doença inflamatória crônica específica que surge no final de tudo isso depende em parte de sua composição genética, em parte dos tipos de exposições que você teve e em parte da composição de seu microbioma intestinal. Conforme explicado por Fasano: 9
“Além da predisposição genética e exposição a gatilhos ambientais, a patogênese de uma variedade de CIDs parece envolver mudanças mutuamente influenciadas na permeabilidade intestinal/tráfico de Ag, ativação imunológica e mudanças na composição / função do microbioma intestinal.
A zonulina é um modulador das funções de barreira epitelial e endotelial … A disbiose intestinal pode causar a liberação de zonulina levando à passagem do conteúdo luminar através da barreira epitelial, causando a liberação de citocinas pró-inflamatórias que causam aumento da permeabilidade estabelecendo uma alça viciosa levando a influxo maciço de Ags dietéticos e microbianos desencadeando a ativação de células T.
Dependendo da composição genética do hospedeiro, as células T ativadas podem permanecer dentro do trato GI, causando CID do intestino … ou migrar para vários órgãos diferentes para causar CID sistêmico. ”
As doenças inflamatórias crônicas associadas à desregulação da via da zonulina incluem:
- Doenças auto-imunes , como doença celíaca, diabetes tipo 1, doença inflamatória intestinal, esclerose múltipla e espondilite anquilosante;
- Doenças metabólicas , como obesidade, resistência à insulina, doença hepática gordurosa não alcoólica, diabetes gestacional, hiperlipidemia e diabetes tipo 2;
- Doenças intestinais , como síndrome do intestino irritável, sensibilidade ao glúten não celíaco e disfunção entérica ambiental (uma doença crônica que afeta o intestino proximal);
- Doenças neuro-inflamatórias , como transtorno do espectro do autismo, esquizofrenia, transtorno depressivo maior e fadiga crônica / encefalomielite miálgica;
- Câncer de cérebro e fígado.
Micróbios intestinais influenciam genes e podem influenciar o risco de câncer
Embora a inclusão do câncer nessa lista possa parecer estranha à primeira vista, alguns pesquisadores acreditam que o microbioma intestinal pode realmente acabar sendo uma virada de jogo para a prevenção e o tratamento do câncer.
Não apenas as bactérias intestinais mostraram influenciar a expressão gênica, 10 , 11 ativando e desativando alguns genes, a pesquisa 12 publicada em 2018 descobriu que os microrganismos intestinais realmente controlam as respostas imunológicas antitumorais em seu fígado e que os antibióticos podem alterar a composição das células imunológicas em seu fígado, desencadeando o crescimento do tumor.
Os pesquisadores da Harvard Medical School identificaram a população específica de micróbios intestinais que modula a resposta imunológica localizada e sistêmica para repelir invasores virais.
Certas bactérias intestinais também promovem a inflamação, que é um fator subjacente a praticamente todos os cânceres, enquanto outras bactérias a suprimem. 13 Foi demonstrado que a presença de certas bactérias intestinais aumenta a resposta do paciente aos medicamentos anti-câncer. 14
Uma maneira pela qual as bactérias intestinais aumentam a eficácia do tratamento do câncer é ativando o sistema imunológico e permitindo que ele funcione com mais eficiência. Na verdade, os pesquisadores descobriram que, quando esses micróbios específicos estão ausentes, certos medicamentos anti-câncer podem não funcionar.
As bactérias intestinais fazem parte da sua defesa antiviral
Bactérias intestinais também estão envolvidas em sua defesa antiviral, mostra uma pesquisa recente 15 . Conforme relatado pela Harvard Medical School, em 18 de novembro de 2020: 16
“Pela primeira vez, os pesquisadores da Harvard Medical School … identificaram a população específica de microrganismos intestinais que modula a resposta imunológica localizada e sistêmica para repelir invasores virais. O trabalho … aponta um grupo de microrganismos intestinais e uma espécie específica dentro deles que faz com que as células imunológicas liberem substâncias químicas repelentes de vírus conhecidas como interferons tipo 1.
Os pesquisadores identificaram ainda a molécula precisa – compartilhada por muitas bactérias intestinais dentro desse grupo – que desbloqueia a cascata de proteção imunológica. Essa molécula, observaram os pesquisadores, não é difícil de isolar e pode se tornar a base para drogas que aumentam a imunidade antiviral em humanos”.
Embora as descobertas ainda precisem ser replicadas e confirmadas, elas apontam para a possibilidade de você ser capaz de aumentar sua imunidade antiviral, semeando novamente seu intestino com Bacteroides fragilis e outras bactérias da família Bacteroides. 17
Essas bactérias iniciam uma cascata de sinalizações que induzem a liberação de interferon-beta que protege contra a invasão viral, estimulando as células do sistema imunológico a atacar o vírus e fazendo com que as células infectadas pelo vírus se autodestruam.
“Especificamente,… uma molécula que reside na superfície da bactéria desencadeia a liberação de interferon-beta ativando a chamada via de sinalização TLR4-TRIF”, explica Harvard. 18 “Esta molécula bacteriana estimula uma via de sinalização imunológica iniciada por um dos nove receptores toll-like (TLR) que fazem parte do sistema imunológico inato.”
O papel da vitamina D
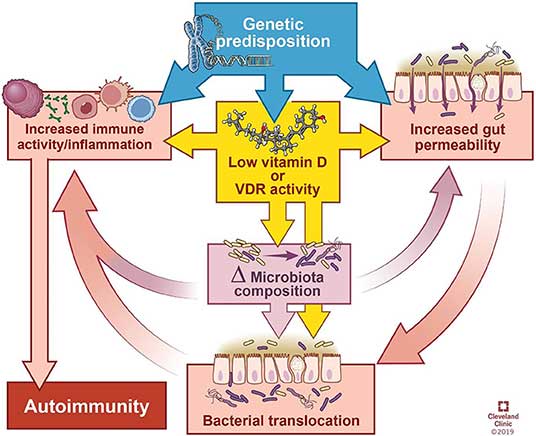
Pesquisas recentes também destacam o papel da vitamina D na saúde intestinal e na auto-imunidade sistêmica. O artigo de revisão, publicado em 21 de janeiro de 2020, em Frontiers in Immunology, observa: 19
“As doenças autoimunes tendem a compartilhar uma predisposição para a deficiência de vitamina D, que altera o microbioma e a integridade da barreira epitelial intestinal.
Nesta revisão, resumimos a influência das bactérias intestinais no sistema imunológico, exploramos os padrões microbianos que surgiram de estudos sobre doenças auto-imunes e discutimos como a deficiência de vitamina D pode contribuir para a auto-imunidade por meio de seus efeitos na função de barreira intestinal, composição do microbioma , e / ou efeitos diretos nas respostas imunológicas.”
Conforme observado nesta revisão, a vitamina D tem vários efeitos regulatórios diretos e indiretos em seu sistema imunológico, incluindo a promoção de células T regulatórias (Tregs), inibindo a diferenciação de células Th1 e Th17, prejudicando o desenvolvimento e a função das células B, reduzindo a ativação de monócitos e estimulando peptídeos antimicrobianos de células imunes.
Dito isso, a relação entre a vitamina D e a auto-imunidade é complicada. Além da imunossupressão, a vitamina D também parece melhorar os distúrbios auto-imunes, pois afeta a composição da microbiota e a barreira intestinal.
A revisão cita pesquisas que mostram que o nível de vitamina D altera a composição do microbioma intestinal. De um modo geral, a deficiência de vitamina D tende a aumentar Bacteriodetes e Proteobacteria, enquanto a maior ingestão de vitamina D tende a aumentar a prevalência de Prevotella e reduzir certos tipos de Proteobacteria e Firmicutes.
Embora as pesquisas ainda sejam escassas no que diz respeito ao impacto da vitamina D nas bactérias intestinais, especialmente em pacientes com doenças auto-imunes, a deficiência de vitamina D e as doenças auto-imunes são comorbidades conhecidas e a suplementação de vitamina D é frequentemente recomendada para esses pacientes.
Vitamina D necessária para manutenção de junção estanque
Mais conhecido é como a vitamina D apoia as defesas das células intestinais e imunológicas no intestino. Na verdade, a vitamina D é um dos componentes cruciais necessários para manter as junções estanques. Conforme explicado nesta revisão: 20
“O epitélio intestinal está em constante interação com o meio externo. A integridade da barreira adequada e a função anti-microbiana nas superfícies epiteliais são críticas na manutenção da homeostase e na prevenção da invasão ou super-colonização de espécies microbianas particulares.
Um epitélio intestinal saudável e uma camada de muco intacta são essenciais para proteger contra a invasão de organismos patogênicos, e a vitamina D ajuda a manter essa função de barreira … Vários estudos descobriram que a sinalização da vitamina D3 / VDR modula a quantidade e distribuição de proteínas de junção apertada …
Como uma proteína ‘permeável’ que permite o movimento de íons no lúmen intestinal, a expressão da claudina-2 no contexto de deficiência funcional de vitamina D pode contribuir para a patologia da colite …
A vitamina D regula positivamente o mRNA do peptídeo antimicrobiano e a expressão de proteínas, incluindo catelicidina, defensinas e lisozima … Peptídeos antimicrobianos, secretados principalmente por células Paneth no intestino, são mediadores importantes da composição do microbioma … As defensinas são secretadas por células epiteliais, células de Paneth e células do sistema imunológico, e são componentes importantes da resposta imune inata no intestino.”
Como a vitamina D pode contribuir para doenças auto-imunes
De acordo com os autores, a deficiência de vitamina D pode contribuir para doenças autoimunes, afetando o microbioma e o sistema imunológico da seguinte maneira:
- A deficiência ou suplementação de vitamina D altera o microbioma e a manipulação da abundância ou composição bacteriana afeta a manifestação da doença.
- A falta de sinalização de vitamina D devido à deficiência alimentar pode prejudicar a integridade da barreira física e funcional do intestino, permitindo assim que as interações bacterianas estimulem ou inibam as respostas imunológicas.
- Suas defesas imunológicas inatas podem ser comprometidas se você for deficiente em vitamina D.
Como otimizar o seu microbioma intestinal
Todas essas informações devem realmente esclarecer que otimizar a flora intestinal e o nível de vitamina D é de importância crucial para uma boa saúde. Ao semear novamente seu intestino com bactérias benéficas, você pode manter micróbios e fungos patogênicos sob controle e evitar que eles assumam o controle e otimizar sua vitamina D ajudará a evitar vazamentos intestinais.
Comer regularmente alimentos tradicionalmente fermentados e cultivados é a maneira mais fácil, eficaz e econômica de causar um impacto significativo no microbioma intestinal. As escolhas saudáveis incluem lassi (uma bebida de iogurte indiano), produtos lácteos orgânicos alimentados com capim cultivado, como kefir e iogurte, natto (soja fermentada) e vegetais fermentados de todos os tipos.
Embora eu não seja um grande defensor da ingestão de muitos suplementos (pois acredito que a maioria dos nutrientes precisa vir dos alimentos), os probióticos são uma exceção se você não comer alimentos fermentados regularmente. Probióticos à base de esporos, ou esporebióticos, podem ser particularmente úteis quando você está tomando antibióticos. Eles também são um excelente complemento para probióticos regulares.
Os esporebióticos, que consistem na parede celular dos esporos do bacilo, ajudarão a aumentar sua tolerância imunológica e, como não contêm nenhuma cepa viva de bacilo, apenas seus esporos – a casca protetora ao redor do DNA e o mecanismo de funcionamento desse DNA – eles são não afetado por antibióticos.
Os antibióticos, como você deve saber, matam indiscriminadamente as bactérias intestinais, boas e más. É por isso que infecções secundárias e diminuição da função imunológica são efeitos colaterais comuns do uso de antibióticos. A exposição crônica a baixas doses de antibióticos por meio da alimentação também prejudica o microbioma intestinal o que pode resultar em doenças crônicas e aumento do risco de resistência aos medicamentos. Por último, mas não menos importante, você também precisa evitar coisas que interrompam ou matem seu microbioma e isso inclui:
- Antibióticos, a menos que seja absolutamente necessário;
- Carnes criadas convencionalmente e outros produtos de origem animal, uma vez que esses animais são rotineiramente alimentados com antibióticos de baixa dosagem, além de grãos geneticamente modificados e / ou tratados com glifosato;
- Alimentos processados (já que o excesso de açúcares alimenta bactérias patogênicas);
- Água clorada e / ou fluoretada;
- Sabão antibacteriano e produtos contendo triclosan.
Fontes e Referências
- 1 Hopkinsmedicine.org, The Gut: Where Bacteria and Immune System Meet
- 2 PLOS ONE 5 de fevereiro de 2010; 5 (2): e9085
- 3, 5, 9 F100Research 2020, 9 (F1000 Faculty Rev): 69
- 4 IFM.org Alessio Fasano
- 6 barreiras de tecido 4: 4, e1251384
- 7, 8 Biomed Network, Zonulin, Gluten, Glyphosate and Tight Junctions
- 10 Mol Cell. 1 de dezembro de 2016; 64 (5): 982-992.
- 11 ScienceDaily 23 de novembro de 2016
- 12 NIH.gov, 24 de maio de 2018
- 13, 14 Nature, 23 de maio de 2018
- 15 Cell, 25 de novembro de 2020; 183 (5): 1312-1324
- 16, 18 Harvard Medical School 18 de novembro de 2020
- 17 Bacteroides Fragilis
- 19, 20 Frontiers in Immunology 21 de janeiro de 2020 DOI: 10.1189 / fimmu.2019.03141
Tradução livre, parcial, de Luiz Jacques Saldanha, janeiro de 2021.


